Thi Online Bài tập Phản ứng oxi hóa - khử có lời giải chi tiết
Bài tập Phản ứng oxi hóa - khử có lời giải chi tiết
-
3641 lượt thi
-
30 câu hỏi
-
40 phút
Câu 1:
Hòa tan hoàn toàn m gam FexOy bằng dung dịch H2SO4 đặc nóng dư thu được khí A và dung dịch B. Cho khi A hấp thụ hoàn toàn vào dung dịch NaOH dư tạo ra 12,6 gam muối. Mặt khác, cô cạn dung dịch B thì thu được 120 gam muối khan. Công thức oxit là:
Đáp án B
Vì H2SO4 đặc nóng dư nên khí A sinh ra là SO2.
Muối khan thu được là
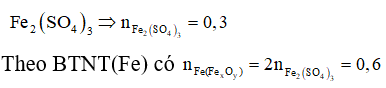
Vì dung dịch NaOH dư nên khỉ dẫn SO2 vào đung dịch NaOH chỉ xảy ra một phản ứng:
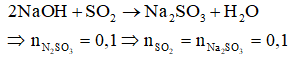
Coi oxit FexOy ban đầu là hỗn hợp của Fe và O.
Gọi nO = a.
Áp dụng định luật bảo toàn moi electron, ta có:
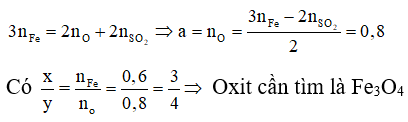
Câu 4:
Cho KI tác dụng với dung dịch KMnO4 trong môi trường H2SO4, người ta thu được 1,51 gam MnSO4 theo phưong trình phản ứng sau: KI + KMnO4 + H2SO4 g I2 +... Số mol I2 tạo thành và số mol KI phản ứng là:
Đáp án B
Bước đầu tiên, cần hoàn thành phương trình phản ứng với đầy đủ các chất và hệ số:
![]()
![]()
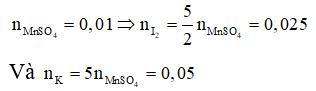
Nhận xét: Ngoài việc viết đầy đủ phản ứng như trên, các bạn vẫn có thể giải quyết bài toán bằng việc áp dụng định luật bảo toàn moi electron và bảo toàn nguyên tố:

Áp dụng định luật bào toàn mol electron, ta có:
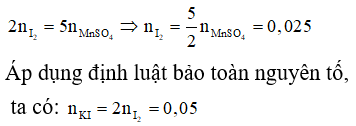
Câu 5:
Hòa tan hoàn toàn m gam Fe3O4 vào dung dịch HNO3 loãng dư, tất cả lượng khí NO thu được được đem oxi hóa thành NO2 rồi sục vào nước cùng dòng khí O2 để chuyển hết thành HNO3. Cho biết thể tích oxi đã tham gia quá trình trên là 3,36 lít. Khối lượng m là:
Đáp án A
Các phản ứng xảy ra:
3Fe3O4 + 28HNO3 g 9Fe(NO3)3 + NO + 14H2O
NO + O2 g NO2
2NO2 + O2 + H2O g2HNO3
Trong toàn bộ quá trình, chỉ có nguyên tố Fe và O thay đổi số oxi hóa (nguyên tố N không có sự thay đổi số oxi hóa). Do đó ta có các quá trình nhường và nhận electron như sau:

Các bài thi hot trong chương:
( 13.3 K lượt thi )
( 8.5 K lượt thi )
( 5 K lượt thi )
( 2.7 K lượt thi )
( 2.3 K lượt thi )
Đánh giá trung bình
0%
0%
0%
0%
0%
