Phân lớp ngoài cùng của hai nguyên tử A, B lần lượt là 3p và 4s; biết tổng số electron của hai phân lớp đó bằng 7 và phân lớp 4s của nguyên tử B chưa bão hòa electron. Nhận định nào sau đây là đúng?
Phân lớp ngoài cùng của hai nguyên tử A, B lần lượt là 3p và 4s; biết tổng số electron của hai phân lớp đó bằng 7 và phân lớp 4s của nguyên tử B chưa bão hòa electron. Nhận định nào sau đây là đúng?
A. A là kim loại, B là khí hiếm.
B. A là phi kim, B là kim loại.
C. A là khí hiếm, B là kim loại.
D. A là khí hiếm, B là phi kim.
Quảng cáo
Trả lời:
Đáp án đúng là: C
Do phân lớp 4s của B chưa bão hòa electron nên B có 1 electron ở phân lớp 4s ⇒ B là kim loại (do có 1 electron ở lớp ngoài cùng).
Số electron trên phân lớp 3p của A là : 7 – 1 = 6.
Cấu hình electron của A là: 1s22s22p63s23p6.
Vậy A là khí hiếm do có 8 electron ở lớp ngoài cùng.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: D
Ta có: Si, P, S, Cl cùng thuộc chu kì 3 trong bảng tuần hoàn.
Theo quy luật biến đổi tính chất ta có tính acid: H2SiO3 < H3PO4 < H2SO4 < HClO4.
Vậy trong 4 acid trên HClO4 có tính acid mạnh nhất.
Lời giải
Đáp án đúng là: B
Độ âm điện là đại lượng đặc trưng cho khả năng hút electron khi hình thành liên kết hóa học.
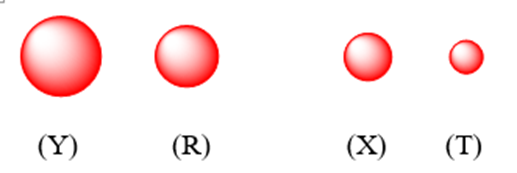
Nguyên tử có bán kính càng nhỏ, độ âm điện càng lớn.
Vậy T có độ âm điện lớn nhất.
Câu 3
A. 15 và 19.
B. 19 và 15.
C. 18 và 15.
D. 19 và 14.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. Số electron ở vỏ nguyên tử của nguyên tố đó là 20.
B. Vỏ của nguyên tử có 4 lớp electron và lớp ngoài cùng có 2 electron.
C. Hạt nhân của calcium có 20 proton.
D. Nguyên tố hóa học này là một phi kim.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. s.
B. d.
C. f.
D. p.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. Acid.
B. Base.
C. Trung tính.
D. Lưỡng tính.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. 1s22s22p4.
B. 1s22s22p63s23p4.
C. 1s22s22p63s23p1.
D. 1s22s22p63s23p3.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.