a) Viết phương trình hóa học của phản ứng xảy ra khi thực hiện phản ứng giữa sodium lần lượt với lượng dư chlorine, oxygen và lưu huỳnh. Giả sử sodium bị oxi hóa hết trong mỗi phản ứng.
b) Cho một lượng nước thích hợp vào mỗi sản phẩm thu được ở ý a) để thu được các dung dịch có nồng độ khoảng 0,1 M. Dự đoán pH của mỗi dung dịch thu được và giải thích.
a) Viết phương trình hóa học của phản ứng xảy ra khi thực hiện phản ứng giữa sodium lần lượt với lượng dư chlorine, oxygen và lưu huỳnh. Giả sử sodium bị oxi hóa hết trong mỗi phản ứng.
b) Cho một lượng nước thích hợp vào mỗi sản phẩm thu được ở ý a) để thu được các dung dịch có nồng độ khoảng 0,1 M. Dự đoán pH của mỗi dung dịch thu được và giải thích.
Câu hỏi trong đề: Bộ 3 đề thi giữa kì 2 Hóa 12 Cánh diều có đáp án !!
Quảng cáo
Trả lời:
a) Phương trình phản ứng:
b) Dự đoán pH dung dịch:
+ Phản ứng (1): pH = 7 do dung dịch NaCl có môi trường trung tính.
+ Phản ứng (2): pH > 7 do Na2O tác dụng H2O tạo thành NaOH có môi trường kiềm.
Na2O + H2O → 2NaOH
+ Phản ứng (3): pH > 7 do Na2S hoàn tan vào H2O, Na2S thủy phân tạo môi trường kiềm.
S2- + H2O ⇌ HS- + OH-
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án: 2,98
Khối lượng đồng giải phóng ở cathode là:
Lời giải
a) Đúng.
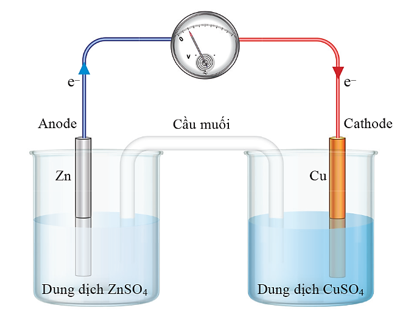
- Ở thanh Zn xảy ra quá trình:
- Ở thanh Cu xảy ra quá trình:
b) Sai. Dòng điện đi qua vôn kế là dòng electron di chuyển từ cực âm (là thanh Zn) sang cực dương (là thanh Cu).
c) Đúng. Cầu muối duy trì tính trung hòa điện của các dung dịch.
d) Đúng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. oxi hóa ion Na+.
B. khử ion Na+.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. Có cấu tạo tinh thể khá rỗng.
B. Có nhiệt độ nóng chảy cao.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.