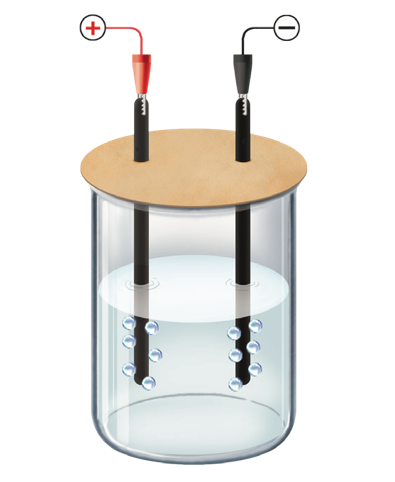
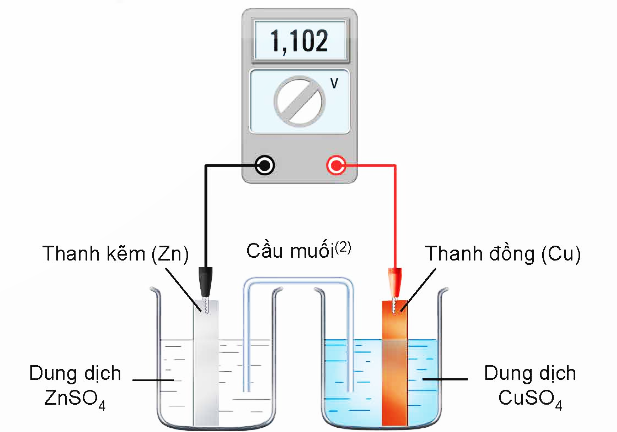
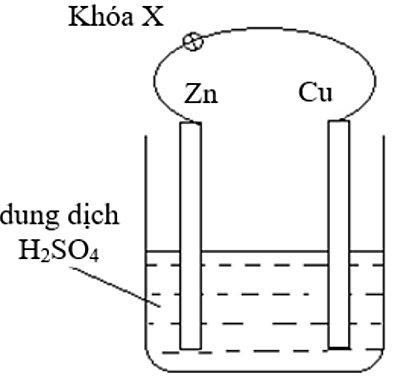
Người ta mạ nickel lên mặt vật kim loại bằng phương pháp mạ điện, dung dịch điện phân chứa \[NiS{O_4},\]cực dương là Ni kim loại, cực âm là vật kim loại cần mạ. Nếu dòng điện có cường độ 1,5 A chạy qua dung dịch trong 2 giờ thì khối lượng nickel được mạ lên vật là bao nhiêu? (Cho biết khối lượng mol của Ni = 58,7 g/mol, hằng số Faraday F = 96500 C/mol, hiệu suất quá trình điện phân là 100%). (Làm tròn kết quả đến hàng phần mười)
Quảng cáo
Trả lời:
Hướng dẫn giải
Đáp án đúng là: 3,3.
Ta có: \(I.t{\rm{ }} = {\rm{ }}{n_e}.F \Rightarrow {n_e} = \frac{{I.t}}{F} = \frac{{1,5.7200}}{{96500}} = 0,1119\,\,mol\)
Phương trình điện phân:
\[\begin{array}{l}N{i^{2 + }}\,\,\,\,\,\,\,\,\,\,\,\, + {\rm{ }}\,\,\,\,\,\,\,\,{\rm{ }}2e{\rm{ }}\,\,\,\,\,\, \to \,\,\,\,\,\,\,\,\,{\rm{ }}Ni\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,1119\,\,\,\,\, \to \,\,\,\,\,\,\,\,\,\frac{{0,1119}}{2}{\rm{ }}mol\end{array}\]
m Ni mạ = \[\frac{{0,1119}}{2}.58,7 \approx 3,3{\rm{ }}g.\]
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hướng dẫn giải
Đáp án đúng là: 1,64
Đổi: 20 cm = 0,2 m; 0,01 mm = 0,001 cm.
\(\begin{array}{l}S = 3,14 \times {(0,2)^2} = 0,1256\;{{\rm{m}}^2} = 1256\;{\rm{c}}{{\rm{m}}^2} \Rightarrow {V_{Ag}} = 1256.0,001 = 1,256(\;{\rm{c}}{{\rm{m}}^3}).\\ \Rightarrow {m_{Ag}} = 1,256.10,5 = 13,188\;({\rm{g)}} \Rightarrow {n_{Ag}} = \frac{{13,188}}{{108}} = 0,1222\;{\rm{mol}}{\rm{.}}\end{array}\)
Ta có: \(Q = {n_e}.F = I.t \Rightarrow t = \frac{{{n_e}.F}}{I} = \frac{{0,1222.96500}}{2} = 5896,5\,\,(s) \simeq 1,64\,(h).\)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. Na+.
B. \[{\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}\].
C. \[{\rm{C}}{{\rm{a}}^{{\rm{2 + }}}}\].
D. \[{{\rm{K}}^{\rm{ + }}}\].
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.