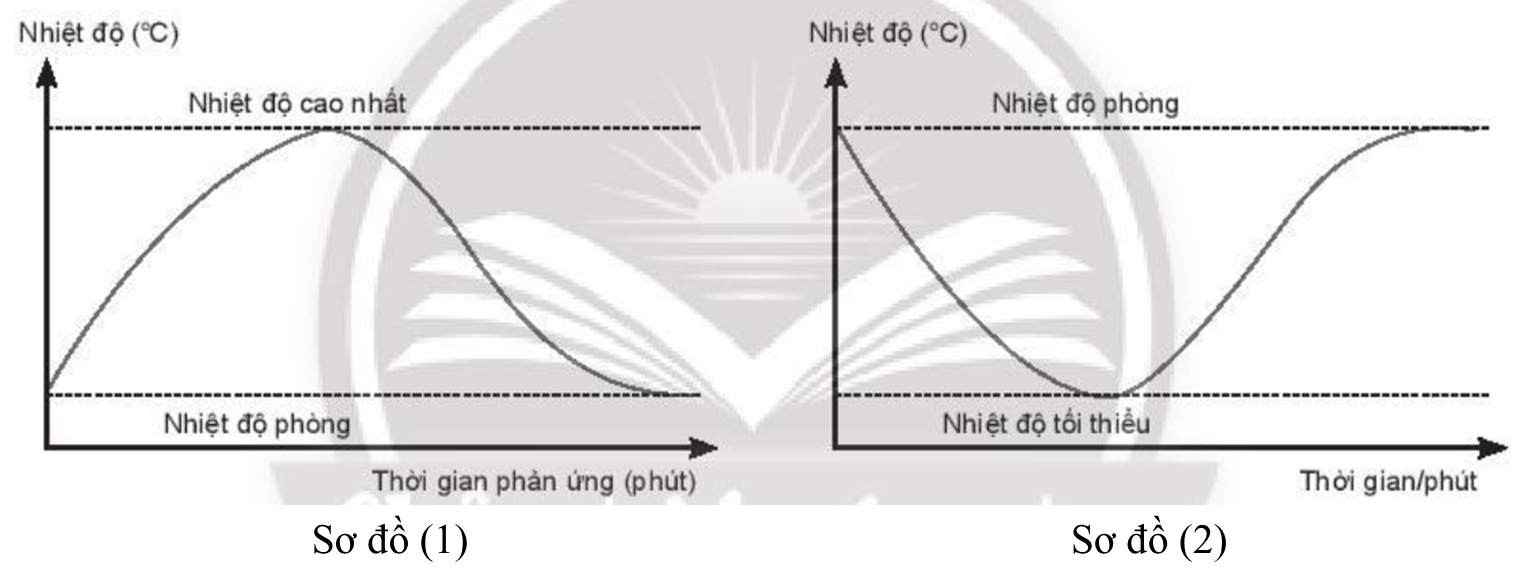
Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình thu nhiệt hay tỏa nhiệt? Theo em, khi pha loãng H2SO4 đặc nên cho từ từ H2SO4 đặc vào nước hay ngược lại? Vì sao?
Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình thu nhiệt hay tỏa nhiệt? Theo em, khi pha loãng H2SO4 đặc nên cho từ từ H2SO4 đặc vào nước hay ngược lại? Vì sao?
Quảng cáo
Trả lời:
Quá trình tỏa nhiệt. Cần nhỏ từ từ H2SO4 đặc vào nước. Nếu làm ngược lại, do phản ứng tỏa nhiệt rất mạnh sẽ làm bắn H2SO4 ra xung quanh, gây mất an toàn và làm hư hại đồ vật, quần áo,…
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Nước hóa rắn: quá trình tỏa nhiệt.
b) Sự tiêu hóa thức ăn: quá trình thu nhiệt.
c) Quá trình chạy của con người: quá trình tỏa nhiệt.
d) Khí CH4 đốt ở trong lò: quá trình tỏa nhiệt.
e) Hòa tan KBr vào nước làm cho nước trở nên lạnh: quá trình thu nhiệt.
g) Sulfuric acid đặc khi thêm vào nước làm cho nước nóng lên: quá trình tỏa nhiệt.
Lời giải
(a) Phản ứng (1) là phản ứng thu nhiệt.
(b) Nhiệt tạo thành chuẩn của H2O(g) là –241,8 kJ/mol.
(c) Biến thiên enthalpy chuẩn của phản ứng 2H2(g) + O2(g) ![]() 2H2O(g) là –483,6 kJ.
2H2O(g) là –483,6 kJ.
(d) Biến thiên enthalpy chuẩn của phản ứng (1) là 241,8 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.