Cho 3 gam Mg vào 100 mL dung dịch HCl nồng độ 1M đến khi phản ứng xảy ra hoàn toàn. Thể tích khí thoát ra (ở 25 °C, 1 bar) là bao nhiêu lít?
A.1,2395.
B. 2,479.
Quảng cáo
Trả lời:
Đáp án đúng là: A
Phương trình hoá học: Mg + 2HCl → MgCl2 + H2
\[{n_{Mg}} = \frac{3}{{24}} = 0,125\,mol;\,{n_{HCl}} = 0,1.1 = 0,1\,mol.\]
Ta có: \[\frac{{{n_{Mg}}}}{1} < \frac{{{n_{HCl}}}}{2}\]nên sau phản ứng HCl hết, Mg dư.
Số mol sản phẩm sinh ra tính theo HCl.
Mg + 2HCl → MgCl2 + H2
0,1→0,050,05mol
Thể tích khí thoát ra (ở 25 °C, 1 bar): 0,05.24,79 = 1,2395 (L)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hướng dẫn giải
Đáp án đúng là: A
Số mol khí H2 là: \({n_{{H_2}}} = \frac{{{V_{{H_2}}}}}{{24,79}} = \frac{{6,72}}{{24,79}} = 0,3\,(mol)\)
PTHH:A + 2HCl \( \to \) ACl2 + H2
0,3 mol 0,3 mol
Theo PTHH ta có: nA = 0,3 mol
⇒\({M_A} = \frac{{{m_A}}}{{{n_A}}} = \frac{{16,8}}{{0,3}} = 56\,(g/mol)\). Kim loại A là Fe.
Câu 2
A. 24,35.
B. 20,05.
C. 12,70.
Lời giải
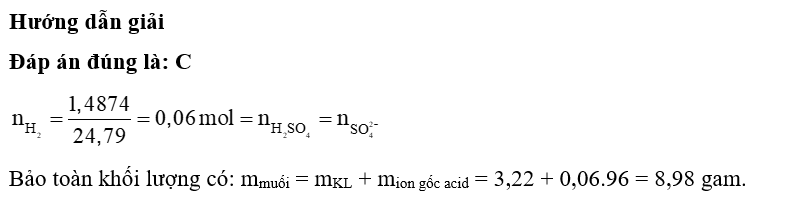
Câu 3
A.1,24 lit.
B. 2,479 lit.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. 13,0 gam.
B. 15,9 gam.
C. 19,5 gam.
D. 26,0 gam.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. 5,6.
B. 11,2.
C. 6,5.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















