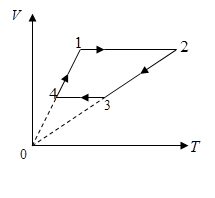Quảng cáo
Trả lời:
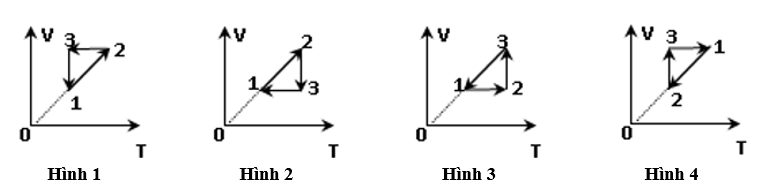
Theo phương trình pV = nRT thì ở đây V và T giống nhau , vậy p tỉ lệ thuận với số mol n. Trong 4 bình đã cho thì bình 1 có số mol lớn nhất , do đó khí ở bình 1 có áp suất lớn nhất .
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Chọn D
Lời giải
a. Đ
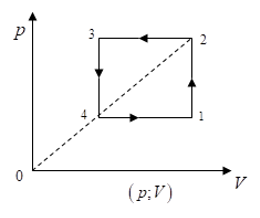
Các quá trình biến đổi trên có hai quá trình biến đổi đẳng tích đó là quá trình (2) sang (3) và quá trình (4) sang (1).
b. Đ
c. S
Từ 3 đến 4 là quá trình đẳng tích, T giảm, p giảm
d. Đ
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.