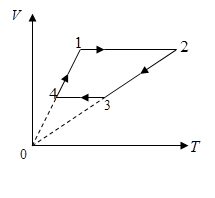Trong xilanh của một động cơ đốt trong có 2dm3 hỗn hợp khí dưới áp suất 175atm và nhiệt độ 47°C. Pit tông nén xuống làm cho thế tích của hỗn hợp khí chỉ còn 0,2 dm3 và áp suất tăng lên 21atm. Tính nhiệt độ của hỗn hợp khí nén theo °C?
Trong xilanh của một động cơ đốt trong có 2dm3 hỗn hợp khí dưới áp suất 175atm và nhiệt độ 47°C. Pit tông nén xuống làm cho thế tích của hỗn hợp khí chỉ còn 0,2 dm3 và áp suất tăng lên 21atm. Tính nhiệt độ của hỗn hợp khí nén theo °C?
Quảng cáo
Trả lời:
Áp dụng công thức: \(\frac{{{p_1}{V_1}}}{{{T_1}}} = \frac{{{p_2}{V_2}}}{{{T_2}}} \Rightarrow {T_2} = \frac{{{p_2}{V_2}.{T_1}}}{{{p_1}{V_1}}} = \frac{{21.0,2\left( {273 + 47} \right)}}{{1,5.2}} = 448K\)
+ Mà \({T_2} = 273 + {t_2} \Rightarrow {t_2} = {175^0}C\)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Chọn D
Lời giải
a. Đ
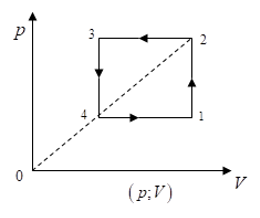
Các quá trình biến đổi trên có hai quá trình biến đổi đẳng tích đó là quá trình (2) sang (3) và quá trình (4) sang (1).
b. Đ
c. S
Từ 3 đến 4 là quá trình đẳng tích, T giảm, p giảm
d. Đ
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.