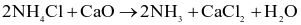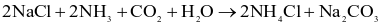Ở điều kiện thường, tinh thể Ca có D = 1,55 g/cm3. Giả thiết các nguyên tử Ca là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng.
Cho biết:
- Công thức tính thể tích hình cầu: V = 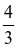 .π.r3
.π.r3
- Số Avogadro NA= 6,023.1023 và số pi π = 3,1416.
Bán kính nguyên tử Ca là bao nhiêu pm? (Làm tròn kết quả đến hàng đơn vị).
Quảng cáo
Trả lời:
Đáp án đúng là: 196.
Trong 1 cm3 tinh thể kim loại Ca thì các quả cầu kim loại chiếm thể tích 0,74 cm3 và có khối lượng 1,55 g.
Số quả cầu kim loại = 6,023 . 1023 . 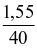 = 0,2334. 1023 = 0,02334 . 1024 (quả)
= 0,2334. 1023 = 0,02334 . 1024 (quả)
Tổng thể tích của quả cầu kim loại là:
V = 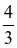 .π.r3.0,02334.1024 = 0,74 → r ≈ 1,96 .10-8cm = 196pm.
.π.r3.0,02334.1024 = 0,74 → r ≈ 1,96 .10-8cm = 196pm.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a. Đúng. 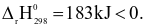 Quá trình Pidgeon là quá trình thu nhiệt.
Quá trình Pidgeon là quá trình thu nhiệt.
b. Đúng. Phương pháp nhiệt luyện dùng để tách các kim loại ra khỏi oxide của chúng bằng các chất khử phù hợp.
c. Đúng. 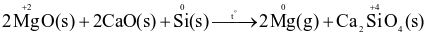
d. Sai.
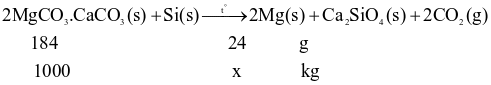
Nếu hiệu suất phản ứng là 90%, thì từ 1 tấn (hay 1000 kg) quặng dolomite sẽ sản xuất được lượng Mg là: 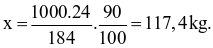
Lời giải
Đáp án đúng là: 850.
Khối lượng đá vôi = 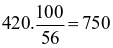 (tấn)
(tấn)
Nhiệt lượng cần cung cấp = 1800.750000 = 1350000000 (kJ)
Khối lượng than đá 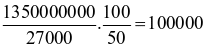 kg = 100 (tấn)
kg = 100 (tấn)
Tổng khối lượng đá vôi và than đá: 750 + 100 = 850 (tấn).
Câu 3
Giá trị biến thiên enthalpy chuẩn của phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA (R) (R(NO3)2(s) 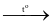 RO(s) + 2NO2(g) +
RO(s) + 2NO2(g) + 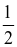 O2(g)) theo bảng sau:
O2(g)) theo bảng sau:
| Muối R(NO3)2(s) | Mg(NO3)2 | Ca(NO3)2 | Sr(NO3)2 | Ba(NO3)2 |
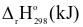
| 255,2 | 369,5 | 452,4 | 506,2 |
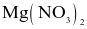 tới
tới
(b) Dựa vào bảng giá trị biến thiên enthalpy chuẩn ở trên có thể dự đoán xu hướng biến đổi độ bền nhiệt của
(c) Phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA  là phản ứng oxi hoá – khử, trong đó vai trò chất oxi hoá là
là phản ứng oxi hoá – khử, trong đó vai trò chất oxi hoá là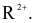
(d) Nhiệt độ phân huỷ theo thứ tự sau: 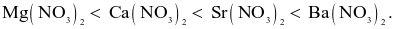
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Một loại nước cứng có thành phần ion như sau:
| Ion | Nồng độ (M) |
| Calcium (Ca2+) | 0,02 |
| Sodium (Na+) | 0,03 |
Hydrogen carbonate (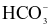 ) )
| x |
(b) Giá trị của x là 0,05.
(c) Có làm mềm mẫu nước cứng trên bằng cách đun nóng.
(d) Để làm mềm 1 lít nước cứng trên, cần dùng ít nhất 40 mL dung dịch NaOH 0,5 M.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt:
MCO3(s) 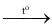 MO (s) + CO2 (g)
MO (s) + CO2 (g)
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
| Muối | MgCO3 (s) | CaCO3 (s) | SrCO3 (s) | BaCO3 (s) |
| ∆rH˚298 (kJ) | 100,70 | 179,20 | 234,60 | 271,50 |
(b) Độ bền nhiệt các muối carbonate của kim loại nhóm IIA tăng dần khi số hiệu nguyên tử của M tăng dần.
(c) Khi để vôi bột (thành phần chính là CaO) lâu ngoài không khí có hiện tượng vôi bột dần bị chuyển hóa lại thành đá vôi (thành phần chính là CaCO3).
(d) Để sản xuất 1 tấn vôi bột theo phương pháp thủ công, người ta nung đá vôi (có hàm lượng CaCO3 là 72%, còn lại là tạp chất trơ) với than đá (giả sử chỉ chứa carbon và tạp chất trơ), biết 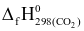 = 393,50 kJ.mol−1. Khi đó, thể tích khí CO2 tối thiểu đã thải ra môi trường ở điều kiện chuẩn nhiều hơn 82,0 m3.
= 393,50 kJ.mol−1. Khi đó, thể tích khí CO2 tối thiểu đã thải ra môi trường ở điều kiện chuẩn nhiều hơn 82,0 m3.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Bán kính nguyên tử giảm dần.
Nhiệt độ nóng chảy tăng dần.
Độ cứng giảm dần.
Khối lượng riêng của đơn chất giảm dần.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















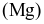 là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:
là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau: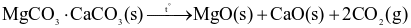
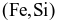 làm chất khử trong điều kiện chân không:
làm chất khử trong điều kiện chân không: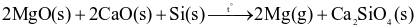
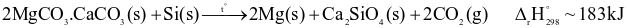
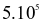 tấn/năm. Phương pháp Solvay với nguyên liệu đầu vào là đá vôi và muối ăn nên giá thành rẻ, phù hợp với sản xuất tại Việt Nam.
tấn/năm. Phương pháp Solvay với nguyên liệu đầu vào là đá vôi và muối ăn nên giá thành rẻ, phù hợp với sản xuất tại Việt Nam.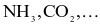
 được tái chế qua phương trình hoá học sau:
được tái chế qua phương trình hoá học sau: