Dựa vào thông tin dưới đây và trả lời các câu hỏi.
Giả sử phản ứng đơn giản: mM + nN → sản phẩm có biểu thức tốc độ phản ứng:
Biểu thức này cho thấy khi nồng độ các chất được giữ không đổi, hằng số tốc độ k tăng (giảm) bao nhiêu lần thì tốc độ phản ứng v cũng tăng (giảm) bấy nhiêu lần. Như vậy, có thể thông qua sự thay đổi giá trị của k để đánh giá sự thay đổi tốc độ phản ứng.
Phương trình Arrehenius giúp chúng ta có thể tính được sự thay đổi của hằng số tốc độ phản ứng k theo năng lượng hoạt hóa và nhiệt độ T (Kelvin).
Trong đó:
A là một hằng số cho một phản ứng xác định.
R là hằng số khí, R = 8,314
Dựa vào thông tin dưới đây và trả lời các câu hỏi.
Giả sử phản ứng đơn giản: mM + nN → sản phẩm có biểu thức tốc độ phản ứng:
Biểu thức này cho thấy khi nồng độ các chất được giữ không đổi, hằng số tốc độ k tăng (giảm) bao nhiêu lần thì tốc độ phản ứng v cũng tăng (giảm) bấy nhiêu lần. Như vậy, có thể thông qua sự thay đổi giá trị của k để đánh giá sự thay đổi tốc độ phản ứng.
Phương trình Arrehenius giúp chúng ta có thể tính được sự thay đổi của hằng số tốc độ phản ứng k theo năng lượng hoạt hóa và nhiệt độ T (Kelvin).
Trong đó:
A là một hằng số cho một phản ứng xác định.
R là hằng số khí, R = 8,314
Phản ứng giữa và là phản ứng đơn giản: (g) + (g) (g). Tốc độ của phản ứng trên được viết dưới dạng:
A. .
B. .
C. .
D. .
Quảng cáo
Trả lời:
Đáp án đúng là: B
Theo thông tin bài đọc, tốc độ của phản ứng trên được viết dưới dạng: .
Câu hỏi cùng đoạn
Câu 2:
Phản ứng của và là phản ứng đơn giản: (g) + (g) 2HI(g). Nếu nồng độ của H2 tăng lên 4 lần thì tốc độ phản ứng thay đổi như thế nào?
A. tăng lên 4 lần.
B. giảm đi 4 lần.
C. tăng lên 16 lần.
D. giảm đi 16 lần.
Đáp án đúng là: A
Phản ứng của H2 và I2 là: H2(g) + I2(g) 2HI(g).
⇒ Tốc độ của phản ứng được viết dưới dạng: .
Nếu nồng độ H2 tăng lên 4 lần thì tốc độ phản ứng khi đó là:
.
⇒ Tốc độ phản ứng tăng lên 4 lần.
Câu 3:
Cho hằng số tốc độ của một phản ứng là tại nhiệt độ 345K và hằng số thực nghiệm Arrhenius là . Năng lượng hoạt hóa của phản ứng trên gần với
A. 1715 mol.
B. 1715
C. 715
D. 715 mol.
Đáp án đúng là: B
Áp dụng phương trình Arrhenius:
⇔ ⇒ Ea ≈ 1714,79 ≈ 1715 kJ/mol.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Chất X có tên là propanone.
Chất X tan được trong nước.
Chất X có 3 đồng phân cấu tạo mạch hở.
Chất X không tạo được kết tủa màu vàng khi cho X vào dung dịch iodine trong NaOH.
Lời giải
Đáp án đúng là: D
X không phản ứng với nước bromine nên X có công thức cấu tạo: CH3COCH3.
Vậy, X là acetone nên tạo được kết tủa màu vàng khi phản ứng với dung dịch iodine trong NaOH.
Câu 2
9,315.
12,420.
6,986.
15,068.
Lời giải
Đáp án đúng là: B
mmethyl salicylate (3,8 triệu tuýp) = 2,7.3,8.106 = 10,26.106 gam = 10,26 tấn.
Khối lượng: 138 g → 152 g
msalicylic acid = tấn 10,26 tấn
Câu 3
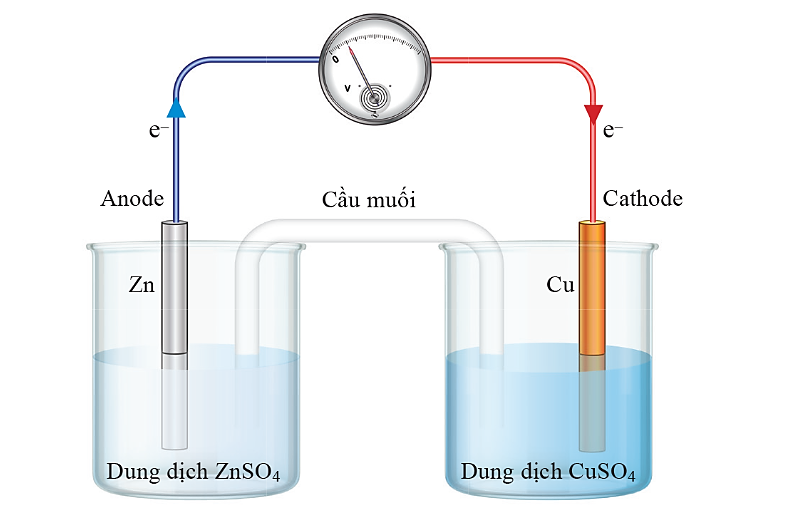
Nồng độ Zn2+ trong dung dịch sẽ tăng lên, còn nồng độ Cu2+ trong dung dịch CuSO4 sẽ giảm xuống.
Dòng điện đi qua vôn kế là dòng electron di chuyển từ cực dương là thanh Cu sang cực âm là thanh Zn.
Trong cầu muối ion K+ sẽ di chuyển vào dung dịch CuSO4 còn ion sẽ di chuyển vào dung dịch ZnSO4.
Nếu điện trở của dây dẫn không đáng kể thì pin mới hoạt động.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
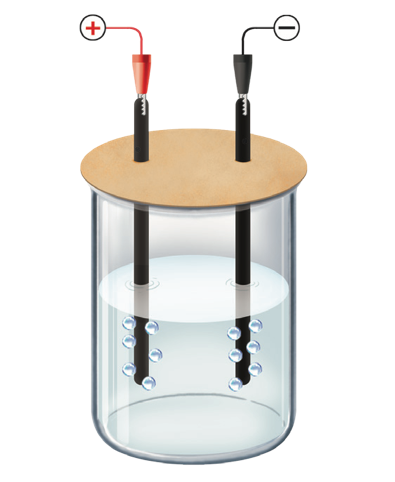
Dung dịch thu được sau điện phân có khả năng tẩy màu.
Thí nghiệm trên được sử dụng để điều chế kim loại Na trong công nghiệp.
Quá trình xảy ra tại cathode là:
Quá trình xảy ra tại anode là:
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.