Nhiệt tạo thành chuẩn () của (s), MgO(s) và (g) được cho lần lượt là –1096,0 kJ·mol⁻¹; –602,0 kJ·mol⁻¹ và –393,5 kJ·mol⁻¹.
Biến thiên enthalpy chuẩn () của phản ứng là bao nhiêu?
100,5 kJ.
494,0 kJ.
+494,0 kJ.
+100,5 kJ.
Quảng cáo
Trả lời:
⇒ = (-602) + (-393,5) – (-1096) = 100,5 kJ.
Chọn D.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
(a) và (b).
(c) và (d).
(a) và (c).
(b) và (d).
Lời giải
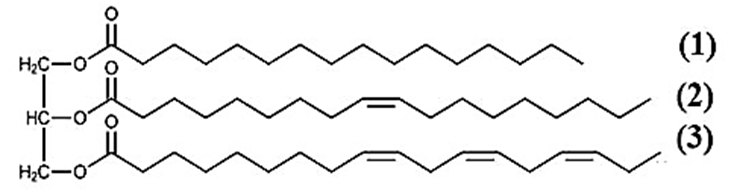
- Phát biểu (a) sai. Phân tử X có 7 liên kết π, trong đó chỉ có các liên kết πC=C là kém bền hơn.
- Phát biểu (b) sai. Acid béo có gốc kí hiệu (3) thuộ̣c loại acid béo omega-3.
- Phát biểu (c) và (d) đúng.
Từ công thức cấu tạo của X, xác định được công thức phân tử của X là:
Chọn B.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
có độ tan kém trong dung dịch phản ứng, dễ dàng kết tinh.
phản ứng oxi hoá - khử xảy ra trong dung dịch.
ở áp suất cao, khí CO2 có thể đẩy Cl− ra khỏi muối NaCl tạo thành
phản ứng trao đổi ưu tiên xảy ra theo chiều thuận để làm giảm số mol khí.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.