Cho các phản ứng sau:
(1) 2H+(aq) + Zn(s) → Zn2+(aq) + H2(g)
(2) Ni(s) + Pb2+(aq) → Ni2+(aq) + Pb(s)
(3) Fe(s) + Mn2+(aq) → Fe2+(aq) + Mn(s)
(4) Cu(s) +2 Ag+(aq)→Cu2+(aq) + 2Ag(s)
| Cặp oxi hoá – khử | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Ag+/Ag | Mn2+/Mn | Ni2+/Ni | 2H+/H2 | Pb2+/Pb |
| Thế điện cực chuẩn (V) | +0,34 | –0,762 | –0,44 | +0,799 | –1,180 | –0,257 | 0,000 | –0,126 |
Liệt kê các phản ứng xảy ra ở điều kiện chuẩn theo số thứ tự tăng dần. (Ví dụ: 123, 234, ...)
Quảng cáo
Trả lời:
Đáp án:
124
Đáp án: 124
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
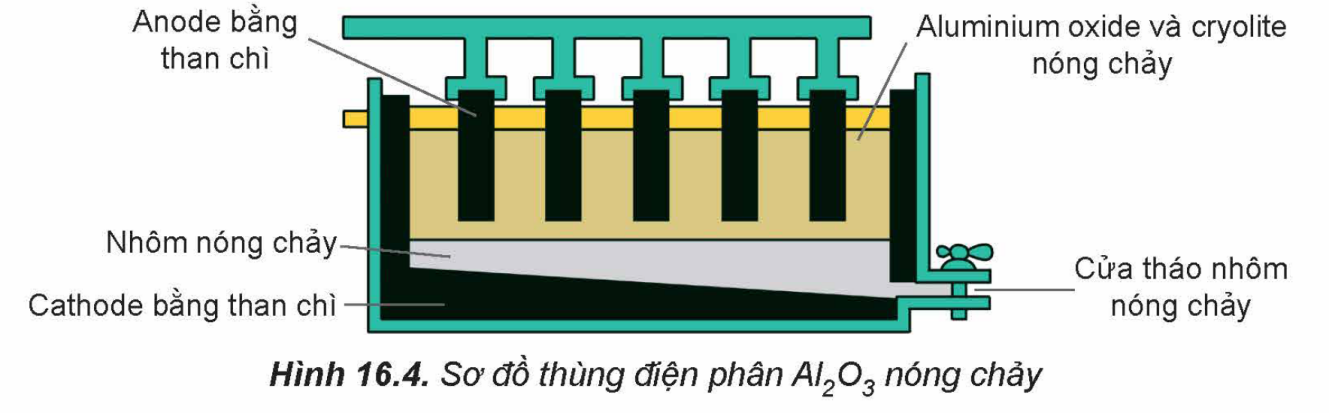
a. Nhôm kim loại được tách ra tại cathode.
b. Khí thoát ra ở anode chủ yếu là O2.
c. Trong công nghiệp có thể thay Al2O3 bằng AlCl3 để tiết kiệm năng lượng, giảm chi phí sản xuất.
d. Để sản xuất được 8 tấn Al (với hiệu suất chuyển hoá Al2O3 thành Al là 90% thì cần 42 tấn quặng bauxite chứa 40% Al2O3 (còn lại là tạp chất không chứa nhôm) (không làm tròn các giai đoạn trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
Lời giải
a. Đúng
b. Sai CO,CO2,…
c. AlCl3 là hợp chất cộng hóa trị, không dẫn điện, bị thăng hoa.
d. Al2O3 → 2Al + \(\frac{3}{2}\) O2
m(bauxite) = \(\frac{m(Al2O3)}{40\%}\) = (\(\frac{8}{27.2.90\%}.102): 40\%\)≈ 42(tấn)
Câu 2
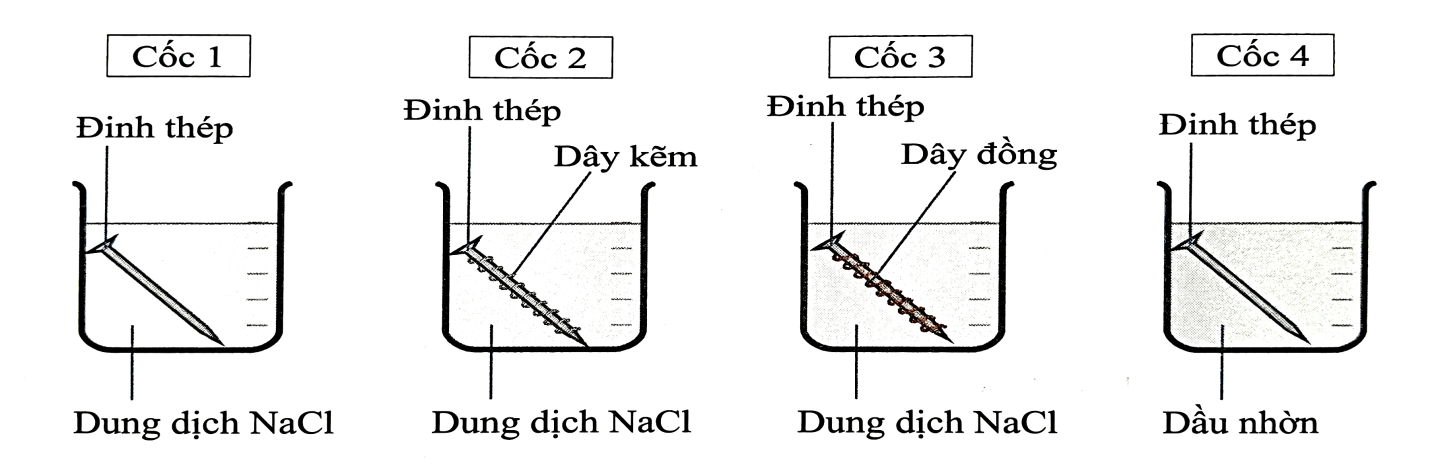
a. Ở cả 4 cốc đều xảy ra hiện tượng ăn mòn điện hoá, và sắt đều đóng vai trò là anode.
b. Ở cốc 1, xảy ra sự hoạt động của vô số các pin điện.
c. Dùng dầu nhờn phủ lên bề mặt kim loại là một trong các phương án để chống ăn mòn kim loại.
d. Nếu tiến hành các thí nghiệm trên trong môi trường chân không thì hiện tượng xảy ra cũng giống như để trong không khí.
Lời giải
a. Sai vì cốc 4 không có ăn mòn điện hóa; cốc 2 sắt là cathode.
b. Đúng vô số pin điện Fe-C.
c. Đúng
d. Sai vì trong môi trường chân không không có ăn mòn còn trong không khí có ăn mòn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
a. Ở bước 3, thêm NaHCO3 vào để trung hoà acid dư.
b. Sau khi bước 4 kết thúc thấy xuất hiện kết tủa đỏ gạch.
c. Dung dịch thu được sau bước 3 có chứa glucose.
d. Có thể thay H2SO4 70% bằng H2SO4 98% để tăng tốc độ, giảm thời gian tiến hành thí nghiệm.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.