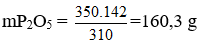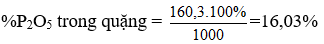Một loại quặng photphat có chứa 35% Ca3(PO4)2. Hãy tính hàm lượng phần trăm P2O5 có trong quặng trên.
Câu hỏi trong đề: Giải Hóa học 11 !!
Quảng cáo
Trả lời:
Trong 1000g quặng có: 1000. 35% = 350g Ca3(PO4)2
Bảo toàn nguyên tố P ⇒ trong 1 mol Ca3(PO4)2 có 1mol P2O5 nghĩa là trong 310g Ca3(PO4)2 tương ứng có 142g P2O5.
⇒350g Ca3(PO4)2 có lượng P2O5 là:
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Ta hoà tan một ít các mẫu phân đạm vào nước thì được 3 dung dịch muối: (NH4)2SO4, NH4Cl, NaNO3. Cho từ từ dung dịch Ba(OH)2 vào từng dung dịch:
- Nếu thấy dung dịch nào có khí bay ra có mùi khai và xuất hiện kết tủa trắng là (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 → BaSO4 ↓ + 2NH3 ↑+ 2H2O
- Nếu thấy dung dịch nào có khí bay ra có mùi khai là NH4Cl
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 ↑+ 2H2O
- Dung dịch không có hiện tượng gì là NaNO3
Lời giải
Phương trình phản ứng:
H3PO4 + NH3 → NH4H2PO4
H3PO4 + 2NH3 → (NH4)2HPO4
⇒ Phương trình phản ứng tổng hợp:
2H3PO4 + 3NH3 → NH4H2PO4 + (NH4)2HPO4
Từ ptpư ta có:
∑số mol NH3 cần dùng = 1,5 số mol H3PO4 = 1,5.6.103 = 9000 (mol)
⇒ VNH3 (đktc) = 9000.22,4 = 201600 (lít)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.