Một nhóm học sinh làm thí nghiệm chế tạo pin điện hóa bằng quả chanh với điện cực bằng Zn và Cu để làm một bóng led sáng rõ được như hình ảnh sau:

Giả thiết để bóng led sáng rõ cần hiệu điện thế tối thiểu là 1,5V, sức điện động đo được của mỗi đơn vị pin trên (tính cho 1 nửa quả chanh) trong điều kiện thí nghiệm là 0,45V.
Cho nước cốt chanh ta có pH ≈ 2,3 còn nước cam có pH ≈ 3,4. Làm thí nghiệm về pin điện hóa như trên lần lượt với quả chanh và quả cam trong cùng điều kiện. Sức điện động của pin tỷ lệ thuận với nồng độ ion H+. Cho các nhận định sau:
(1) Sức điện động làm từ quả chanh lớn hơn làm từ quả cam.
(2) Để pin hoạt động hiệu quả hơn nên bóp quả chanh để các các tép chanh vỡ ra thuận lợi cho sự dẫn điện.
(3) Quá trình chủ yếu xảy ra tại cực dương của pin là 2H+ + 2e → H2.
(4) Nếu giữ nguyên các lá Zn, thay các lá Cu bằng Sn thì bóng led sẽ sáng rõ hơn.
Nhận định sai là
Nhận định (4).
Nhận định (3).
Nhận định (2).
Nhận định (1).
Quảng cáo
Trả lời:
Đáp án đúng là A
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
Đáp án: 1043
- số mol Na2CO3:
- Xét các phản ứng:
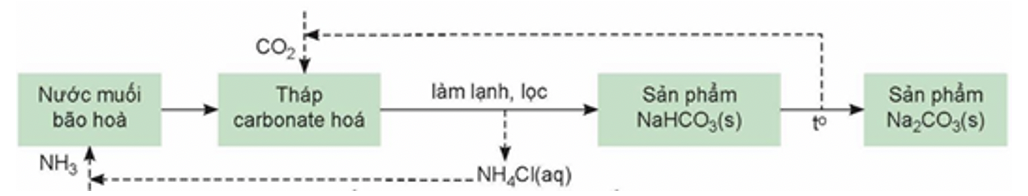
CaCO3 CaO + CO2 (1)
NaCl + NH3 + CO2 + H2O NaHCO3 + NH4Cl (2)
2NaHCO3 Na2CO3 + CO2 (1)
- Vì lượng CO2 được bảo toàn suốt quá trình nên toàn bộ CO2 sinh ra sẽ chuyển hóa vào Na2CO3
Khối lượng của CaCO3:
- Khối lượng của đá vôi:
Câu 2
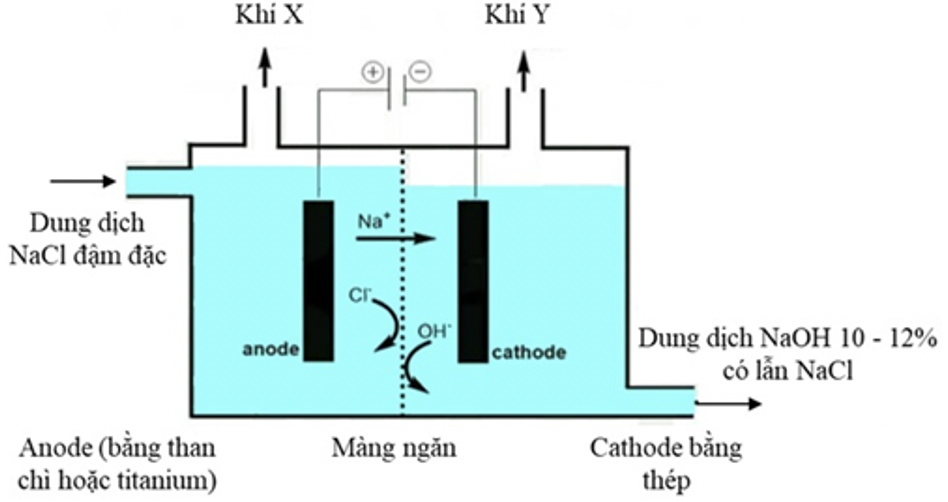
a. Phương trình hoá học của phản ứng điện phân: 2NaCl(aq) + 2H2O(aq) → Cl2(g) + H2(g) + 2NaOH(aq)
b. Để thu được dung dịch NaOH tinh khiết hơn (nồng độ 50%) có thể tăng nồng độ dung dịch NaCl ban đầu.
c. Ở cathode, nước bị khử thay vì Na+ do thế điện cực chuẩn của cặp 2H+/H2 cao hơn Na+/Na.
d. Tiến hành điện phân liên tục 5,00 giờ với dòng điện không đổi 25,0 kA (hiệu suất dòng cho cả 2 điện cực là 96,5%) 2000 kg dung dịch muối ăn NaCl 25% được cấp vào ngăn anode. Dung dịch thu được ở cathode là NaOH 12,0% khối lượng, chứa 2,0% NaCl (do rò rỉ và kéo theo). Khối lượng NaCl còn lại ở anode là 214,83125 kg. Biết trong quá trình điện phân, màng ngăn không đảm bảo nên đã có 5% Cl2 sinh ra phản ứng với NaOH.
Lời giải
a) Đúng
b) Sai. NaCl ban đầu là dung dịch bão hòa nên không thể tăng nồng độ được nữa.
c) Sai. Ở cathode, nước bị khử thay vì Na+ do thế điện cực chuẩn của cặp 2H2O/ H2 + 2OH- cao hơn Na+/Na.
d) Đúng
- Số mol electron trao đổi:
- Khối lượng dung dịch NaOH 12% thu được sau khi điện phân:
- Khối lượng muối NaCl bị rò rỉ kéo theo:
- Khối lượng NaCl còn lại ở anode:
Câu 3
HCl.
NaNO3.
NaCl.
Na2CO3.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
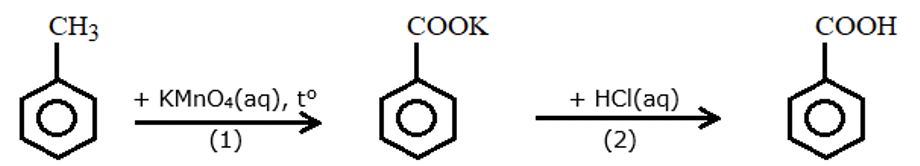
a. Giá trị của h là 60,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười).
b. Trong phản ứng với KMnO4(aq) ở giai đoạn (1), toluene đóng vai trò là chất oxi hoá.
c. Trên phổ hồng ngoại của benzoic acid, tín hiệu (peak) ở 1690 cm-1 đặc trưng cho liên kết O-H.
d. Trong phản ứng ở giai đoạn (2), anion C6H5COO- là một base theo thuyết Brønsted – Lowry.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Dung dịch AgNO3.
Dung dịch MgCl2.
Dung dịch ZnCl2.
Dung dịch CuCl2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.