Formic acid là một chất lỏng, mùi xốc mạnh và gây bỏng da, acid này được chưng cất lần đầu từ loài kiến lửa có tên là Formicarufa. Kiến khi cắn sẽ “tiêm” dung dịch chứa 50% thể tích formic acid vào da. Trung bình mỗi lần cắn, kiến có thể “tiêm” khoảng 6,0.10-3 cm³ dung dịch formic acid. Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate (NaHCO3). Tính khối lượng sodium hydrogencarbonate (mg) cần dùng để trung hoà hoàn toàn lượng formic acid từ vết kiến cắn (biết khối lượng riêng của formic acid là 1,22 g/cm³). (Kết quả làm tròn đến hàng phần mười).
Quảng cáo
Trả lời:
Đáp án:
Đáp án: 6,7
NaHCO3 + HCOOH -> HCOONa + H2O
Thể tích acid là: 6.10-3.0,5=3.10-3(l)
Khối lượng acid là: 3.10-3.1,22=3,66.10-3(g)
Số mol acid là: \(\frac{0.00366}{46}\)=7,957.10-5(mol)
=> khối lượng muối: 84. 7,957.10-5=6,7.10-3(g)=6,7(mg)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
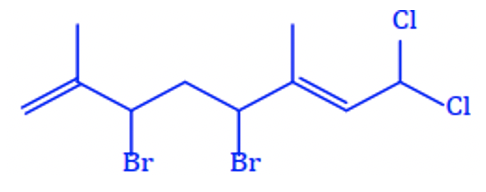
a. Dẫn xuất halogen trên có tên là 1,1-dichloro-4,6-dibromo-3,7-dimethylocta-1,6-diene.
b. Phần trăm khối lượng của nguyên tố chlorine trong dẫn xuất halogen trên bằng 19,45%.
c. Công thức phân tử của dẫn xuất halogen là C10H14Cl2Br2.
d. Số liên kết π trong phân dẫn xuất halogen trên bằng 2.
Lời giải
a) Sai
b) Đúng
Đếm được 10C, 2Cl, 2Br, 2 liên kết π
Gọi x là số nguyên tử H trong 1 phân tử
Ta có:
\(\frac{10.2-x-2-2+2}{2}=2\) => x=14
=> %mCl=\(\frac{35,5.2}{12.10+14+80.2+35,5.2}.100=19,45\%\)
c) Đúng
d) Đúng
Câu 2
a. Hiện tượng phú dưỡng sẽ làm lượng oxygen trong nước hồ giảm đi.
b. Nước hồ sau khi xử lý có nồng độ NH4+ là 8 mg/L, đạt quy chuẩn kỹ thuật quốc gia về nước thải khi thải vào các nguồn nước không dùng cho mục đích cấp nước sinh hoạt.
c. Khối lượng khí chlorine tối thiểu dùng để oxi hóa hoàn toàn NH3 trong bước (2) là 946,67 kg (Làm tròn đến hàng phần trăm).
d. Ở bước 1, khi tác dụng với nước vôi trong, ammonium (NH4+) thể hiện tính khử.
Lời giải
a) Đúng
b) Đúng
c) Đúng
5000m3=5.106l
Ta có: hàm lượng NH4+ là 40mg/l => m=40.5.106=2.108(mg)=2.105(g)
=> n=\(\frac{200000}{14+4}(mol)\), H=80% => số mol tham gia phản ứng là: \(\frac{200000.80}{18.100}=\frac{160000}{18}(mol)\)
NH4+ + OH- -> NH3 + H2O
Số mol OH- = số mol NH4+ tham gia phản ứng = \(\frac{160000}{18}\)(mol)
2NH3 + 3Cl2 -> N2 + 6HCl
Số mol Cl2 là: \(\frac{3.160000}{2.18}\)=946,67.103(g)=946,67(kg)
d) Sai
Câu 3
(CH3)2HC+.
CH3H2C+.
(CH3)3C+.
H3C+.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
CH3C6H4NH2.
C6H5CH=CH2.
C6H5COOH.
C6H5C2H5.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















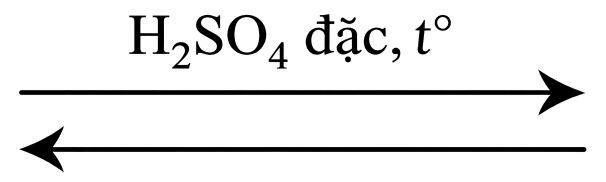 HOC6H4COOCH3 + H2O
HOC6H4COOCH3 + H2O