Trong bình phản ứng (có dung tích không đổi), ban đầu chứa N2O4 và NO2 với nồng độ mol/L bằng nhau. Xảy ra phản ứng thuận nghịch: N2O4(g) ⇌ 2NO2(g)
Tại thời điểm cân bằng, nồng độ N2O4 giảm đi một nửa so với ban đầu. Phần trăm số mol NO2 trong hỗn hợp ở trạng thái cân bằng là
70%.
80%.
60%.
90%.
Quảng cáo
Trả lời:
Đáp án đúng là B
Ban đầu 1 1 (mol)
Cân bằng 0,5 2
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
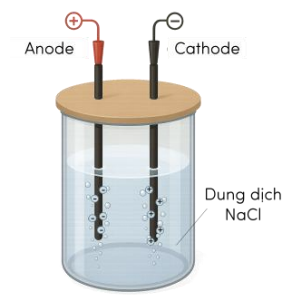
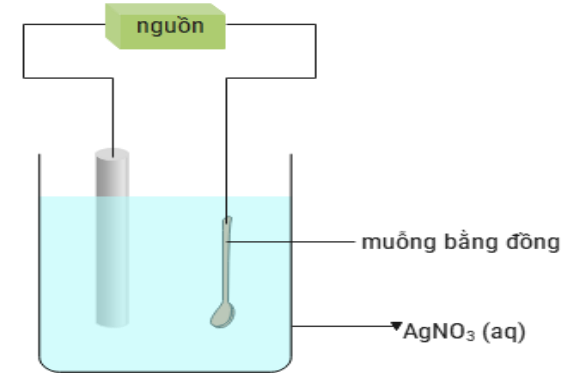
Kết thúc thí nghiệm, cánh hoa hồng bị mất màu.
Tại điện cực cathode xảy ra quá trình oxi hoá nước: H2O + 2e → 2OH- + H2
Tại điện cực anode có khí Cl2 thoát ra.
Dùng nắp đậy trong quá trình điện phân để hạn chế sự thoát Cl2 ra ngoài môi trường gây độc hại cho người làm thí nghiệm và ô nhiễm môi trường.
Lời giải
a. Đúng. Cánh hoa hồng bị mất màu, do không có màng ngăn giữa 2 cực nên sản phẩm tạo thành ở hai điện cực khuếch tán vào nhau sẽ xảy ra phản ứng hoá học tạo thành nước Javel có tính tẩy màu.
b. Sai. Vì tại điện cực cathode xảy ra quá trình khử nước: 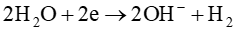
c. Đúng. Dùng nắp đậy trong quá trình điện phân để tăng hiệu suất phản ứng tạo nước Javel, hạn chế sự thoát Cl2 ra ngoài môi trường gây độc hại cho người làm thí nghiệm và ô nhiễm môi trường.
d. Đúng.
Câu 2
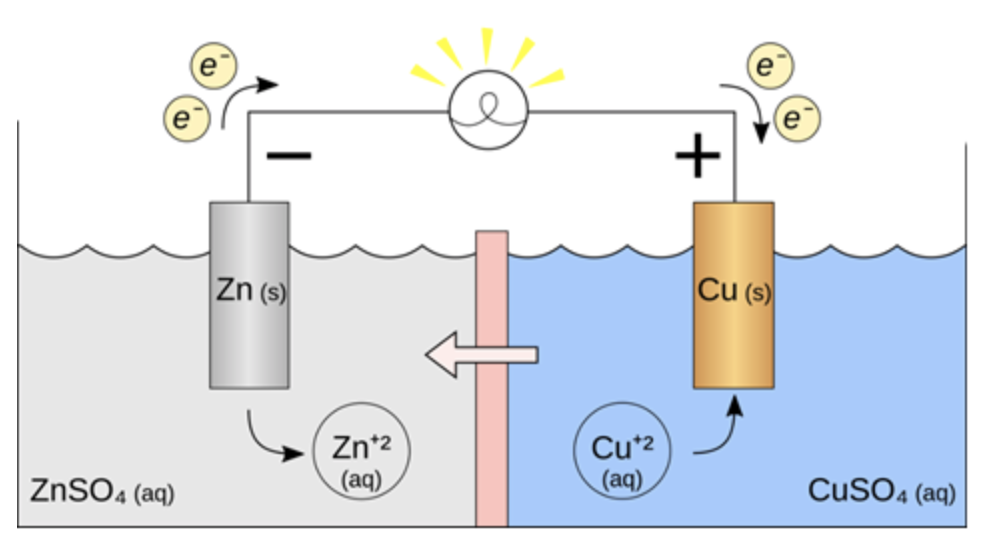
Sử dụng một pin Galvani với điện cực Zn – Cu để thắp sáng một bóng đèn nhỏ với cường độ dòng điện chạy qua là I = 0,02A. Nếu điện cực kẽm hao mòn 0,05 mol do pin phóng điện thì thời gian tối đa mà pin thắp sáng được bóng đèn là 268 giờ. (Kết quả được làm tròn đến hàng đơn vị). Biết Q = I.t = n.F, trong đó: Q là điện lượng (C), n là số mol electron đi qua dây dẫn, I là cường độ dòng điện (A), t là thời gian (giây), F là hằng số Faraday (96500 C/mol).
Khối lượng điện cực zinc (Zn) giảm nhiều hơn khối lượng điện cực copper (Cu) tăng.
Nồng độ SO42- (aq) trong dung dịch ZnSO4 giảm dần và trong dung dịch CuSO4 tăng dần.
Sức điện động chuẩn của pin là 1,103V.
Lời giải
a) Sai, số mol Zn hao mòn 0,05 mol; t= = ≈ 134 giờ.
b) Đúng. Khối lượng Zn giảm là 0,05x65 = 3,25 gam; Khối lượng Cu tăng là 0,05 x64 = 3,2 gam.
c) Sai, anion SO42- di chuyển qua màng để cân bằng điện tích trong dung dịch.
d) Đúng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
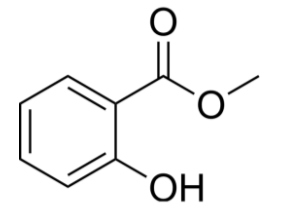
Cho 13,8 gam salicylic acid phản ứng với 20 mL methanol (D = 0,79 g/mL), sau phản ứng thu được 11,4 gam methyl salicylate khi đó hiệu suất phản ứng đạt 70%.
1 mol methyl salicylate tác dụng tối đa với 2 mol NaOH trong dung dịch.
Trong quá trình tinh chế sản phẩm, có thể sử dụng MgSO4 khan (hoặc Na2SO4 khan) để loại nước còn lẫn trong sản phẩm sau phản ứng.
Phản ứng (1) là phản ứng ester hóa.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
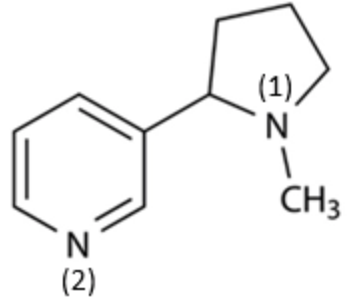
Trong phân tử nicotine, nguyên tử N số (1) là amine bậc hai.
Phần trăm về khối lượng carbon trong nicotine là 74,07%.
Nicotine thuộc loại amine thơm có chứa vòng benzene.
Công thức phân tử của nicotine là C10H15N2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.