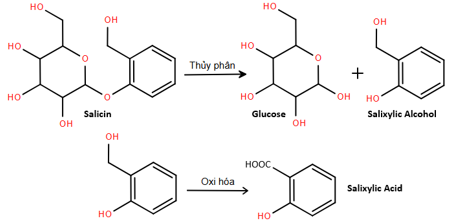
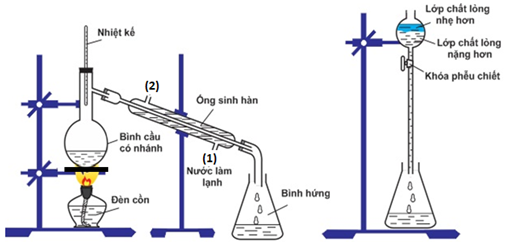
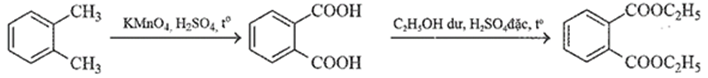Để tiến hành mạ một tấm huy chương hình trụ, đáy tròn với bán kính 2,5 cm; chiều cao hình trụ 0,3 cm; với lớp mạ bằng copper dày 0,1 cm như hình bên.
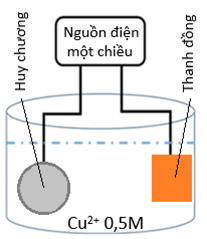
Người ta có thể tiến hành điện phân dung dịch X (CuSO4) nồng độ 0,5M, dư với cường độ dòng điện không đổi 2A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t giây. Biết khối lượng riêng của copper là 8,95 g/cm³ và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng copper tạo ra đều bám hết vào tấm huy chương. Cho hằng số Faraday F = 96500, π = 3,14.
Thanh copper là cực dương, huy chương được mạ sẽ đóng vai trò cực âm.
Khi kết thúc điện phân bên điện cực anode thoát ra 8,193 lít (đkc).
Chiều dòng electron di chuyển từ huân chương được mạ qua dây dẫn đến thanh copper.
Thời gian điện phân 64800 giây.
Quảng cáo
Trả lời:
a) Đúng
b) Sai, tại anode: Cu → Cu2+ + 2e, không có khí O2 thoát ra.
c) Sai, chiều dòng electron di chuyển từ thanh Cu, qua nguồn điện đến tấm huy chương. Nguồn điện đóng vai trò giống như “máy bơm” electron.
d) Sai
Trước mạ: r = 2,5 cm; h = 0,3 cm → V = 5,8875 cm³
Sau khi mạ: r = 2,5 + 0,1 = 2,6 cm; h = 0,3 + 0,1.2 = 0,5 cm → V = 10,6132
(Công thức V = πr²h, trong đó π = 3,14)
→ mCu = 8,95(V sau – V trước) = 42,295015 gam
mCu = 64It/2F → t = 63773s
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Kim loại hy sinh luôn có thế điện cực chuẩn cao hơn kim loại cần được bảo vệ.
Nếu thanh kẽm không tiếp xúc hoặc không nối với thanh sắt thì nó không bảo vệ được thanh sắt khỏi bị ăn mòn.
Sắt bị gỉ nhanh hơn khi tiếp xúc với kẽm nhưng bị gỉ chậm hơn khi tiếp xúc với đồng.
Trong một thí nghiệm nghiên cứu sự ảnh hưởng của các yếu tố đến khả năng sử dụng kẽm để bảo vệ chống ăn mòn thép. Một khối kẽm có khối lượng 25,0 gam được gắn lên một thiết bị bằng thép đặt trong nước biển. Sau một thời gian, cân lại thì thấy khối lượng của kẽm là 28,0 gam. Giả thiết trong quá trình làm việc, toàn bộ Zn chỉ bị oxi hóa thành Zn(OH)2 và hydroxide này bám hết lên khối kẽm. Phần trăm khối lượng kẽm đã bị oxi hóa là 22,94%. (Kết quả cuối cùng làm tròn đến hàng phần trăm)
Lời giải
a) Sai, kim loại hy sinh phải có tính khử mạnh hơn kim loại cần bảo vệ, do đó nó phải có thế điện cực chuẩn thấp hơn kim loại cần được bảo vệ.
b) Đúng, dòng electron phải di chuyển từ thanh Zn sang thanh Fe thì quá trình bảo vệ mới tồn tại. Dòng electron di chuyển này có thể thông qua tiếp xúc trực tiếp hoặc thông qua dây dẫn.
c) Sai, tính khử Zn > Fe > Cu, do đó khi tiếp xúc với Zn thì Fe được bảo vệ, khi tiếp xúc với Cu thì Fe lại trở thành kim loại hy sinh.
d) Đúng:
nOH(trong Zn(OH)2) = (28 – 25)/17 = 3/17
→ nZn bị oxi hóa = nZn(OH)2 = 3/34
→ %Zn bị oxi hóa = (65.3/34)/25 = 22,94%
Lời giải
Đáp án:
Đáp án: 1,46
(RCOO)3C3H5 + 3CH3OH → 3RCOOCH3 + C3H5(OH)2
mCH3OH = 10.3.32/830 = 96/83 kg
→ V = (96/83)/0,79 = 1,46L
(Coi như tỉ lệ ban đầu đúng bằng tỉ lệ đã phản ứng).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Trong phân tử diethyl phthalate có tổng cộng 3 liên kết π.
Cho 1 mol diethyl phthalate tác dụng hết 2 mol NaOH thu được 1 mol alcohol và 2 mol muối.
Diethyl phthalate thuộc loại ester đa chức (diester).
Để sản xuất được 5 triệu hộp DEP (quy cách 10 gam/hộp, hoạt chất DEP chiếm 88,8% khối lượng) với hiệu suất cả quá trình là 80%, cần lượng tối thiểu 26,5 tấn o-dimethylbenzene.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.