Để chuẩn bị cho buổi thực hành vào sáng hôm sau, một giáo viên đã pha dung dịch KMnO4 có nồng độ 0,05 M dùng làm chất chuẩn. Tuy nhiên, do thời tiết nắng nóng, dung dịch có dấu hiệu bị phân hủy. Vì vậy, trước khi bắt đầu giờ thực hành, giáo viên đã tiến hành xác định lại nồng độ chính xác của dung dịch này theo các bước sau:
• Bước 1: Hòa tan 1,512 gam tinh thể H2C2O4.2H2O bằng nước cất, sau đó chuyển vào bình định mức 100 mL và thêm nước đến vạch thu được dung dịch X.
• Bước 2: Lấy chính xác 10,00 mL dung dịch X cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H2SO4 2M. Sau đó, đun nóng nhẹ dung dịch trong bình tam giác đến khoảng 70°C.
• Bước 3: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 ở trên đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng lại. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,70 mL.
Phương pháp chuẩn độ tuân theo phương trình hóa học (chưa cân bằng) sau:
H2C2O4 + KMnO4 + H2SO4 → K2SO4 + MnSO4 + CO2 + H2O
Có thể thay thế dung dịch H2SO4 bằng dung dịch HCl để làm môi trường cho phản ứng.
Chất chỉ thị trong phép chuẩn độ trên là dung dịch KMnO4.
Nồng độ thực tế của dung dịch KMnO4 tại thời điểm chuẩn độ đã giảm 1,03% so với nồng độ ban đầu khi mới pha. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm).
Nồng độ mol của H2C2O4 trong dung dịch X đã pha chế ở bước 1 là 0,12M.
Quảng cáo
Trả lời:
a) Sai, không thể thay thế dung dịch H2SO4 bằng dung dịch HCl do Cl- có tính khử sẽ xảy ra phản ứng:
10Cl- + 2MnO4- + 16H+ → 5Cl2 + 2Mn2+ + 8H2O
b) Đúng, bản thân ion MnO4- có màu tím đậm, khi bị khử thành Mn2+ thì không màu. Tại điểm tương đương, chỉ cần dư một giọt KMnO4, dung dịch sẽ chuyển sang màu hồng nhạt bền vững (MnO4- ở nồng độ rất thấp sẽ có màu hồng).
c) Đúng:
5H2C2O4 + 2KMnO4 + 3H2SO4 → K2SO4 + 2MnSO4 + 10CO2 + 8H2O
nH2C2O4.2H2O ban đầu = 1,512/126 = 0,012 mol = 12 mmol
→ nH2C2O4 (10 mL X) = 1,2 mmol
→ nKMnO4 (9,70 mL) = 0,48 mmol
→ CM KMnO4 = 0,48/9,70 = 0,049485M
Độ giảm = (0,05 – 0,049485)/0,05 = 1,03%
d) Đúng, CM H2C2O4 = 12/100 = 0,12M
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là B
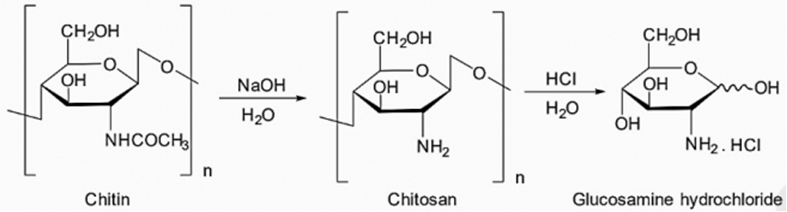
Sơ đồ: (C8H13O5N)n → nC6H14ClNO5
mC6H14ClNO5 = 1000.10.12.1500 = 180000000 mg = 180 kg
→ m vỏ tôm = 180.203/(215,5.28%.40%) = 1514 kg
Câu 2
Một nhà máy dược phẩm sản xuất thuốc nhỏ mắt chứa muối sodium của HA – sodium hyaluronate nồng độ 0,1% (khối lượng/thể tích). Từ 1 kg nguyên liệu thô chứa 2,5% sodium hyaluronate về khối lượng, nhà máy thu được 2500 lọ thuốc nhỏ mắt (loại 10 mL mỗi lọ). Biết rằng, hiệu suất của toàn bộ quá trình đạt 80%.
HA tồn tại ở dạng polyanion (tích điện âm) trong điều kiện sinh lí cơ thể (pH ~ 7,4).
Trong phân tử HA, các đơn vị monosaccharide chi liên kết với nhau bằng liên kết β-1,4-glycoside.
HA là một polymer thiên nhiên thuộc loại polysaccharide tạp chức.
Lời giải
a) Sai: mHA trong nguyên liệu = 1000.2,5% = 25 gam
Thể tích thuốc mắt pha chế được = 25.80%/0,1% = 20000 mL
Khi đóng lọ 10 mL thì số lọ = 20000/10 = 2000 lọ
Chú ý: Nồng độ khối lượng/thể tích là số gam chất tan có trong 100 mL dung dịch.
→ HA 0,1% nghĩa là có 0,1 gam HA trong 100 mL dung dịch.
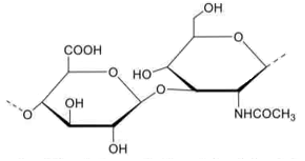
b) Đúng, trong mỗi mắt xích HA có các nhóm:
+ Nhóm chức alcohol: Không thể phân li thành H+.
+ Nhóm chức amide: -CO-NH-, trong nhóm này liên kết π của C=O đã liên hợp với đôi electron tự do chưa liên kết của N nên tính base của N gần như đã bị vô hiệu hóa hoàn toàn.
+ Nhóm chức -COOH: Có thể phân li ra H+
Như vậy mỗi mắt xích của HA gần như một acid đơn chức, ở pH = 7,4 đa số các nhóm -COOH đã mất proton để trở thành anion, và toàn phân tử HA trở thành polyanion.
c) Sai:
+ Liên kết β-1,3-glycoside: Nối D-glucuronic acid với N-acetyl-D-glucosamine trong nội bộ mắt xích.
+ Liên kết β-1,4-glycoside: Nối N-acetyl-D-glucosamine của mắt xích này với D-glucuronic acid của mắt xích kế ngay sau nó.
d) Đúng, HA là một polysaccharide thiên nhiên, có trong cơ thể người, tập trung nhiều ở dịch khớp, thủy tinh thể và da. Nó là một dạng polysaccharide mở rộng (dẫn xuất của polysaccharide), khác với polysaccharide nguyên thủy chỉ có C, H, O. Với nhiều loại nhóm chức, HA là hợp chất tạp chức.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
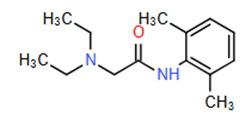
C2H5N(CH3)CH2COOH.
C2H5N(C2H5)CH2COOH.
CH3N(C2H5)CH2COONa.
C2H5N(C2H5)CH2COONa.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
a. Nồng độ ion H+ của nước bể bơi đo được ở bước 2 gấp 2,51 lần nồng độ ion H+ của dung dịch chuẩn có pH = 10,01.
b. Nước trong bể bơi tại thời điểm đo đang ở trạng thái không an toàn.
c. Biết rằng, giá trị sức điện động phụ thuộc tuyến tính vào pH dung dịch theo dạng phương trình y = ax + b. Ở bước 2, sức điện động mà máy đo ghi nhận được có giá trị xấp xỉ -23,6 mV.
d. Ở bước 1, sức điện động của hệ có xu hướng giảm khi nồng độ H+ trong dung dịch giảm.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
a. Trên phổ IR của methyl alcohol sẽ xuất hiện tín hiệu có số sóng trong vùng 3650 – 3200 cm-1.
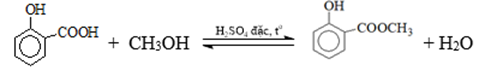
b. Dựa vào sự biến mất của tín hiệu có số sóng trong vùng 3300 – 2500 cm-1 trên phổ IR, có thể kiểm tra xem salicylic acid đã phản ứng hết hay chưa.
c. Tiến hành đun hồi lưu hỗn hợp chứa 0,69 gam salicylic acid và 5 mL methyl alcohol (d = 0,79 g/mL) với xúc tác H2SO4 đậm đặc. Sau quá trình tinh chế, nếu lượng methyl salicylate tinh khiết thu được là 0,57 gam thì hiệu suất của quá trình tổng hợp đạt 75,0%.
d. Trong phân tử methyl salicylate có chứa nhóm chức alcohol.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.