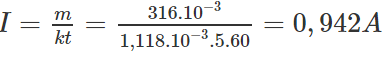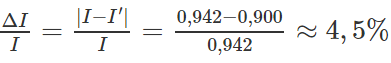Một ampe kế được mắc nối tiếp với bình điện phân chứa dung dịch bạc nitrat () và số chi của nó là 0,90 A. Số chỉ này có đúng không, nếu dòng điện chạy qua bình điện phân trong khoảng thời gian 5,0 phút đã giải phóng 316 mg bạc tới bám vào catôt của bình này. Đương lượng điện hoá của bạc (Ag) là 1,118 mg/C.
Câu hỏi trong đề: Giải Sách Bài Tập Vật Lí 11 !!
Quảng cáo
Trả lời:
Theo định luật I của Fa-ra-đây về điện phân, khối lượng bạc tới bám vào catôt tính bằng :
m = kIt
Từ đó suy ra dòng điện chạy qua bình điện phân phải có cường độ :
là chưa đúng và kết quả đo của ampe kế có sai số tỉ đối bằng :
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Cường độ dòng điện I = 0,05.t (A) thay đổi tăng dần đều trong khoảng thời gian từ = 0 đến = 1 phút = 60 s ứng với các giá trị cường độ dòng điện và = 0,05.60 = 3,0 A. Do đó, điện lượng chuyển qua dung dịch đồng sunphat có giá trị trung bình bằng :
Áp dụng công thức Fa-ra-đây về điện phân, ta xác định được khối lượng đồng bám vào catôt của bình điện phân :
Lời giải
Đáp án B
Khối lượng của niken được giải phóng ra ở điện cực của bình điện phân tuân theo định luật I Fa-ra-đây :
m = kq = kIt
trong đó k là đương lượng điện hoá của niken, q = It là điện lượng chuyển qua dung dịch điện phân.
Thay số, ta tìm được : m = 0,3..5,0.3600 = 5,4g.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.