Nung m gam Al trong 6,72 lít O2. Chất rắn thu được sau phản ứng cho hoà tan hết vào dung dịch HCl thấy bay ra 6,72 lít H2 (các thể tích khí đo ở đktc). Giá trị của m là
Nung m gam Al trong 6,72 lít O2. Chất rắn thu được sau phản ứng cho hoà tan hết vào dung dịch HCl thấy bay ra 6,72 lít H2 (các thể tích khí đo ở đktc). Giá trị của m là
A. 8,1.
Quảng cáo
Trả lời:
Đáp án B
Phương pháp giải:
Chất rắn thu được sau phản ứng chứa Al dư phản ứng với dung dịch HCl tạo khí H2.
Dựa vào phương trình hóa học của 2 phản ứng (Al + O2 và Al + HCl) ⟹ nAl ⟹ m.
Giải chi tiết:
nO2 = nH2 = 6,72/22,4 = 0,3 (mol)
PTHH: 4Al + 3O2 2Al2O3
Theo PTHH ⟹ nAl(pứ) = 4nO2/3 = 0,4 (mol).
Chất rắn thu được sau phản ứng gồm Al (dư) và Al2O3.
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 ↑
Theo PTHH ⟹ nAl = 2nH2/3 = 2.0,3/3 = 0,2 (mol).
⟹ ΣnAl = 0,4 + 0,2 = 0,6 (mol) ⟹ m = 0,6.27 = 16,2 gam.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án D
Phương pháp giải:
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ phương trình (1)
+) Ta có nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa (theo x, y)
Mà nAl pư = nOH- ⟹ phương trình (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ phương trình (3)
Giải hệ được x; y; z ⟹ giá trị của m.
Giải chi tiết:
nH2 = = 0,12 mol.
Chất rắn là Al dư ⟹ nAl dư = = 0,03 mol.
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ z = 9x (1)
+) nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa = 2x + y (mol)
Mà nAl pư = nOH- ⟹ 2x + y = z - 0,03 (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ 2x + y + 3.(z - 0,03) = 2.0,12 (3)
Giải hệ (1)(2)(3) được: x = 0,01; y = 0,04; z = 0,09.
⟹ m = 0,01.137 + 0,04.23 + 0,09.27 = 4,72 gam.
Câu 2
A. 11,08.
Lời giải
Đáp án C
Phương pháp giải:
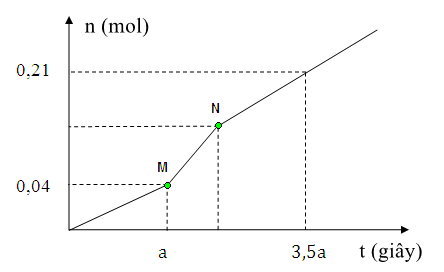
Chia đồ thị ra 3 giai đoạn
Đoạn 1: chỉ có Cl2 thoát ra ở anot
Đoạn 2: Có Cl2 và H2 bên catot thoát ra
Đoạn 3: Có H2 và O2 bên anot thoát ra
Lập phương trình với số mol khí thoát ra và số mol e trao đổi sẽ tìm ra được số mol mỗi khí Cl2, H2, O2
Từ đó suy ngược lại tìm được m.
Giải chi tiết:
Tại catot: Tại anot:
Cu2+ + 2e → Cu 2Cl- → Cl2 + 2e
H2O + 2e → H2 + 2OH- H2O → O2 + 4H+ + 4e
Đoạn 1: nCl2 = 0,04 mol
→ Trong a giây mỗi điện cực đã trao đổi 0,04.2 = 0,08 mol electron.
Đoạn 2: Có độ dốc lớn hơn đoạn 1 nên tốc độ thoát khí nhanh hơn → thoát Cl2 và H2
Bảo toàn electron → nCl2 = nH2 = u (mol)
Đoạn 3: Thoát H2 và O2. Đặt nO2 = v mol → nH2 = 2v mol
Ta có hệ:
nCuSO4 = nCu = nCl2 đoạn 1 = 0,04 (mol)
nNaCl = 2nCl2 tổng = 2(0,04 + 0,04) = 0,16(mol)
→ m = 0,04.160 + 0,16.58,5 = 15,76 (g)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Khí H2S và khí Cl2.
B. Khí NH3 và khí HCl.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. KOH.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. 7,06.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.