Phát biểu nào sau đây sai?
Phát biểu nào sau đây sai?
A. Dùng CO khử Al2O3 nung nóng, thu được Al.
B. Nối thanh kẽm với vỏ tàu biển bằng thép thì vỏ tàu được bảo vệ.
C. Natri cacbonat là muối của axit yếu.
Quảng cáo
Trả lời:
Đáp án A
Phương pháp giải:
Dựa vào kiến thức tổng hợp về chương 5,6 (Hóa 12).
Giải chi tiết:
A sai vì CO chỉ khử được oxit kim loại sau nhôm (dãy điện hóa).
B đúng vì kẽm có tính khử mạnh hơn sắt (thép) nên bị ăn mòn trước.
C đúng vì CO32- là gốc của axit yếu H2CO3.
D đúng.
PTHH: Ba + 2H2O → Ba(OH)2 + H2 ↑
Ba(OH)2 + CuSO4 → BaSO4 ↓ + Cu(OH)2 ↓
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án D
Phương pháp giải:
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ phương trình (1)
+) Ta có nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa (theo x, y)
Mà nAl pư = nOH- ⟹ phương trình (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ phương trình (3)
Giải hệ được x; y; z ⟹ giá trị của m.
Giải chi tiết:
nH2 = = 0,12 mol.
Chất rắn là Al dư ⟹ nAl dư = = 0,03 mol.
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ z = 9x (1)
+) nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa = 2x + y (mol)
Mà nAl pư = nOH- ⟹ 2x + y = z - 0,03 (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ 2x + y + 3.(z - 0,03) = 2.0,12 (3)
Giải hệ (1)(2)(3) được: x = 0,01; y = 0,04; z = 0,09.
⟹ m = 0,01.137 + 0,04.23 + 0,09.27 = 4,72 gam.
Câu 2
A. 11,08.
Lời giải
Đáp án C
Phương pháp giải:
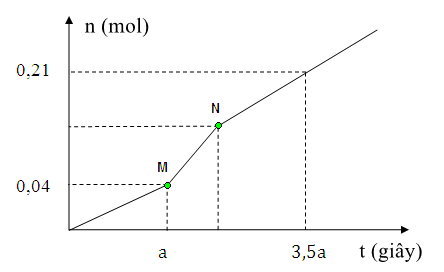
Chia đồ thị ra 3 giai đoạn
Đoạn 1: chỉ có Cl2 thoát ra ở anot
Đoạn 2: Có Cl2 và H2 bên catot thoát ra
Đoạn 3: Có H2 và O2 bên anot thoát ra
Lập phương trình với số mol khí thoát ra và số mol e trao đổi sẽ tìm ra được số mol mỗi khí Cl2, H2, O2
Từ đó suy ngược lại tìm được m.
Giải chi tiết:
Tại catot: Tại anot:
Cu2+ + 2e → Cu 2Cl- → Cl2 + 2e
H2O + 2e → H2 + 2OH- H2O → O2 + 4H+ + 4e
Đoạn 1: nCl2 = 0,04 mol
→ Trong a giây mỗi điện cực đã trao đổi 0,04.2 = 0,08 mol electron.
Đoạn 2: Có độ dốc lớn hơn đoạn 1 nên tốc độ thoát khí nhanh hơn → thoát Cl2 và H2
Bảo toàn electron → nCl2 = nH2 = u (mol)
Đoạn 3: Thoát H2 và O2. Đặt nO2 = v mol → nH2 = 2v mol
Ta có hệ:
nCuSO4 = nCu = nCl2 đoạn 1 = 0,04 (mol)
nNaCl = 2nCl2 tổng = 2(0,04 + 0,04) = 0,16(mol)
→ m = 0,04.160 + 0,16.58,5 = 15,76 (g)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Khí H2S và khí Cl2.
B. Khí NH3 và khí HCl.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. 7,06.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. KOH.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.