Este hai chức, mạch hở X có công thức phân tử C6H8O4 và không tham gia phản ứng tráng bạc. X được tạo thành từ ancol Y và axit cacboxylic Z. Dung dịch Y không phản ứng với Cu(OH)2 ở điều kiện thường; khi đun Y với H2SO4 đặc ở 170oC không tạo ra anken. Nhận xét nào sau đây đúng?
Este hai chức, mạch hở X có công thức phân tử C6H8O4 và không tham gia phản ứng tráng bạc. X được tạo thành từ ancol Y và axit cacboxylic Z. Dung dịch Y không phản ứng với Cu(OH)2 ở điều kiện thường; khi đun Y với H2SO4 đặc ở 170oC không tạo ra anken. Nhận xét nào sau đây đúng?
A. Phân tử X có chứa một nhóm metyl.
B. Chất Y là ancol etylic.
C. Phân tử Z có số nguyên tử cacbon bằng số nguyên tử oxi.
Quảng cáo
Trả lời:
Đáp án C
Phương pháp giải:
Độ bất bão hòa ⟹ Số liên kết π trong X.
- X không tráng gương ⟹ X không có đầu HCOO-
- Y không tác dụng Cu(OH)2, to thường ⟹ Y không có nhiều nhóm OH kề nhau.
- Y không tạo được anken ⟹ Y là ancol đa chức (C ≤ 3) hoặc Y là CH3OH.
- Mà X có CTPT là C6H8O4; X tạo thành từ ancol Y và axit cacboxylic Z
⟹ CTCT của X, Y, Z.
Giải chi tiết:
Độ bất bão hòa ⟹ X có chứa 3 liên kết π.
- X không tráng gương ⟹ X không có đầu HCOO-
- Y không tác dụng Cu(OH)2, to thường ⟹ Y không có nhiều nhóm OH kề nhau.
- Y không tạo được anken ⟹ Y là ancol đa chức (C ≤ 3) hoặc Y là CH3OH.
- Mà X có CTPT là C6H8O4; X tạo thành từ ancol Y và axit cacboxylic Z
⟹ X: CH3OOC-CH=CH-COOCH3 hoặc CH3OOC-C(=C)-COOCH3.
Y: CH3OH.
Z: HOOC-CH=CH-COOH
A sai, X có 2 nhóm CH3.
B sai, Y là CH3OH.
C đúng, Z là HOOC-CH=CH-COOH.
D sai, Z có liên kết C=C nên làm mất màu dung dịch Br2.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án D
Phương pháp giải:
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ phương trình (1)
+) Ta có nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa (theo x, y)
Mà nAl pư = nOH- ⟹ phương trình (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ phương trình (3)
Giải hệ được x; y; z ⟹ giá trị của m.
Giải chi tiết:
nH2 = = 0,12 mol.
Chất rắn là Al dư ⟹ nAl dư = = 0,03 mol.
Đặt nBa = x; nNa = y; nAl = z (mol).
+) nAl = 9nBa ⟹ z = 9x (1)
+) nOH- = 2nBa(OH)2 + nNaOH = 2nBa + nNa = 2x + y (mol)
Mà nAl pư = nOH- ⟹ 2x + y = z - 0,03 (2)
+) Áp dụng bảo toàn e: 2nBa + nNa + 3nAl pư = 2nH2 ⟹ 2x + y + 3.(z - 0,03) = 2.0,12 (3)
Giải hệ (1)(2)(3) được: x = 0,01; y = 0,04; z = 0,09.
⟹ m = 0,01.137 + 0,04.23 + 0,09.27 = 4,72 gam.
Câu 2
A. 11,08.
Lời giải
Đáp án C
Phương pháp giải:
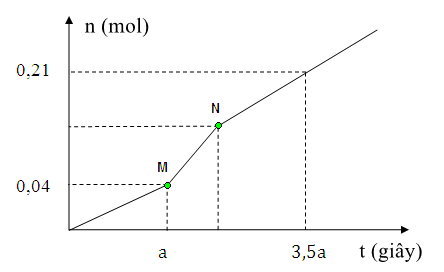
Chia đồ thị ra 3 giai đoạn
Đoạn 1: chỉ có Cl2 thoát ra ở anot
Đoạn 2: Có Cl2 và H2 bên catot thoát ra
Đoạn 3: Có H2 và O2 bên anot thoát ra
Lập phương trình với số mol khí thoát ra và số mol e trao đổi sẽ tìm ra được số mol mỗi khí Cl2, H2, O2
Từ đó suy ngược lại tìm được m.
Giải chi tiết:
Tại catot: Tại anot:
Cu2+ + 2e → Cu 2Cl- → Cl2 + 2e
H2O + 2e → H2 + 2OH- H2O → O2 + 4H+ + 4e
Đoạn 1: nCl2 = 0,04 mol
→ Trong a giây mỗi điện cực đã trao đổi 0,04.2 = 0,08 mol electron.
Đoạn 2: Có độ dốc lớn hơn đoạn 1 nên tốc độ thoát khí nhanh hơn → thoát Cl2 và H2
Bảo toàn electron → nCl2 = nH2 = u (mol)
Đoạn 3: Thoát H2 và O2. Đặt nO2 = v mol → nH2 = 2v mol
Ta có hệ:
nCuSO4 = nCu = nCl2 đoạn 1 = 0,04 (mol)
nNaCl = 2nCl2 tổng = 2(0,04 + 0,04) = 0,16(mol)
→ m = 0,04.160 + 0,16.58,5 = 15,76 (g)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Khí H2S và khí Cl2.
B. Khí NH3 và khí HCl.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. 7,06.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. KOH.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.