Thực hiện hai thí nghiệm dưới đây:
Thí nghiệm 1: Đặt một nhiệt kế vào trong cốc thủy tinh chứa khoảng 50 ml dung dịch hydrochloric acid (HCl) 1M (hình 14.1). Khi nhiệt độ trong cốc ổn định, ghi nhiệt độ ban đầu. Thêm vào cốc khoảng 1 gam magnesium oxide (MgO) rồi dùng đũa thủy tinh khuấy liên tục. Quan sát hiện tượng phản ứng và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Thí nghiệm 2: Lặp lại thí nghiệm với bộ dụng cụ và cách tiến hành như trên, nhưng thay bằng khoảng 50 ml dung dịch CH3COOH 5% (giấm ăn) và khoảng 5 gam baking soda (sodium hydrogen carbonate, NaHCO3). Quan sát và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Viết phương trình hóa học xảy ra ở hai thí nghiệm trên và cho biết phản ứng nào là tỏa nhiệt, phản ứng nào là thu nhiệt.
Thực hiện hai thí nghiệm dưới đây:
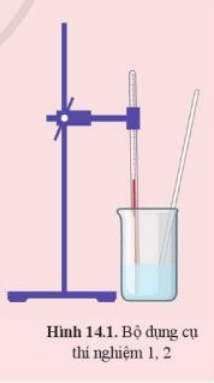
Thí nghiệm 1: Đặt một nhiệt kế vào trong cốc thủy tinh chứa khoảng 50 ml dung dịch hydrochloric acid (HCl) 1M (hình 14.1). Khi nhiệt độ trong cốc ổn định, ghi nhiệt độ ban đầu. Thêm vào cốc khoảng 1 gam magnesium oxide (MgO) rồi dùng đũa thủy tinh khuấy liên tục. Quan sát hiện tượng phản ứng và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Thí nghiệm 2: Lặp lại thí nghiệm với bộ dụng cụ và cách tiến hành như trên, nhưng thay bằng khoảng 50 ml dung dịch CH3COOH 5% (giấm ăn) và khoảng 5 gam baking soda (sodium hydrogen carbonate, NaHCO3). Quan sát và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Viết phương trình hóa học xảy ra ở hai thí nghiệm trên và cho biết phản ứng nào là tỏa nhiệt, phản ứng nào là thu nhiệt.

Câu hỏi trong đề: Bài tập Phản ứng hóa học và enthalpy có đáp án !!
Quảng cáo
Trả lời:
Học sinh làm thí nghiệm và ghi lại sự thay đổi nhiệt độ trong quá trình phản ứng.
Thí nghiệm 1:
Phương trình hóa học: MgO(s) + 2HCl(aq) → MgCl2(aq) + H2O(l)
Hiện tượng: MgO tan trong dung dịch HCl.
Thí nghiệm 2:
Phương trình hóa học: CH3COOH + NaHCO3 → CH3COONa + H2O + CO2
Hiện tượng: Bột baking soda (sodium hydrogen carbonate, NaHCO3) tan trong dung dịch giấm ăn (CH3COOH). Có khí không màu, không mùi thoát ra.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
A. Nhiệt tạo thành của HCl là -184,6 kJ mol-1
Phát biểu B và C là đúng
H2(g) + Cl2(g) → 2HCl(g) (*) ∆ r = - 184,6 kJ
Cách 1: Tính enthalpy tạo thành chuẩn của HCl dựa vào enthalpy của phản ứng
∆ r = 2. ∆ f(HCl(g)) - ∆ r(H2(g)) - ∆ r(H2(g))
⇔ - 184,6 = 2. ∆ f(HCl(g)) – 0 – 0
⇒ ∆ f(HCl(g)) = -92,3 kJ mol-1
Cách 2: Tính enthalpy tạo thành chuẩn của HCl dựa vào định nghĩa.
Phản ứng tạo thành 2 mol HCl(g) ở điều kiện chuẩn tỏa ra 184,6 kJ
⇒ Phản ứng tạo thành 1 mol HCl(g) ở điều kiện chuẩn tỏa ra = 92,3 kJ
⇒ ∆ f(HCl(g)) = -92,3 kJ mol-1
Lời giải
1 gam C2H2(g) tương ứng với mol C2H2(g)
Đốt cháy hoàn toàn mol C2H2(g) giải phóng 50,01 kJ nhiệt lượng
Vật đốt cháy hoàn toàn 1 mol C2H2 sẽ giải phóng 50,01.26 = 1300,26 kJ nhiệt lượng
Phản ứng: C2H2(g) + O2(g) → 2CO2(g) + H2O(l) ∆ r = -1300,26 kJ
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















