Cho vị trí của các nguyên tố E, T, Q, X, Y, trong bảng tuần hoàn rút gọn (chỉ biểu diễn các nguyên tố nhóm A) như sau:
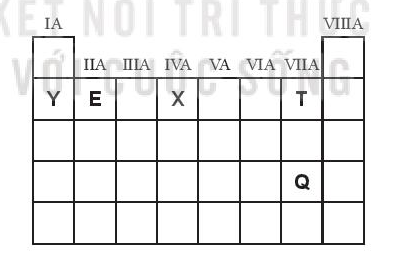
Có các nhận xét sau:
(1) Thứ tự giảm dần tính kim loại là Y, E, X.
(2) Thứ tự tăng dần độ âm điện là Y, X, T.
(3) Thứ tự tăng dần tính phi kim là T, Q.
(4) Thứ tự giảm dần bán kính nguyên tử Y, E, X, T.
Số nhận xét đúng là
Cho vị trí của các nguyên tố E, T, Q, X, Y, trong bảng tuần hoàn rút gọn (chỉ biểu diễn các nguyên tố nhóm A) như sau:

Có các nhận xét sau:
(1) Thứ tự giảm dần tính kim loại là Y, E, X.
(2) Thứ tự tăng dần độ âm điện là Y, X, T.
(3) Thứ tự tăng dần tính phi kim là T, Q.
(4) Thứ tự giảm dần bán kính nguyên tử Y, E, X, T.
Số nhận xét đúng là
A. 1
B. 2
C. 3
D. 4
Câu hỏi trong đề: Bài tập Ôn tập chương 2 có đáp án !!
Quảng cáo
Trả lời:
Đáp án C
(1) Đúng vì trong một chu kì tính kim loại giảm theo chiều tăng của điện tích hạt nhân nguyên tử.
(2) Đúng vì theo chiều tăng của điện tích hạt nhân nguyên tử: trong một chu kì độ âm điện tăng dần.
⇒ Thứ tự tăng dần độ âm điện là Y, X, T.
(3) Sai vì trong một nhóm tính phi kim giảm dần theo chiều tăng của điện tích hạt nhân nguyên tử.
⇒ Thứ tự tăng dần tính phi kim là Q, T.
(4) Đúng vì trong 1 chu kì bán kính nguyên tử giảm dần theo chiều tăng của điện tích hạt nhân nguyên tử.
⇒ Thứ tự giảm dần bán kính nguyên tử là Y, E, X, T.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Borax (Na2B4O7.10H2O), còn gọi là hàn the, là khoáng chất dạng tinh thể. Nhờ có khả năng hoà tan oxide của kim loại, borax được dùng để làm sạch bề mặt kim loại trước khi hàn, chế tạo thuỷ tinh quang học, men đồ sứ... Một lượng lớn borax được dùng để sản xuất bột giặt.
a) Nêu vị trí trong bảng tuần hoàn của mỗi nguyên tố có trong thành phần của borax và viết cấu hình electron của nguyên tử các nguyên tố đó.
b) Sắp xếp các nguyên tố trên (trừ H) theo chiều bán kính nguyên tử tăng dần và giải thích.
c) Sắp xếp các nguyên tố trên (trừ H) theo chiều độ âm điện giảm dần và giải thích.
Borax (Na2B4O7.10H2O), còn gọi là hàn the, là khoáng chất dạng tinh thể. Nhờ có khả năng hoà tan oxide của kim loại, borax được dùng để làm sạch bề mặt kim loại trước khi hàn, chế tạo thuỷ tinh quang học, men đồ sứ... Một lượng lớn borax được dùng để sản xuất bột giặt.
a) Nêu vị trí trong bảng tuần hoàn của mỗi nguyên tố có trong thành phần của borax và viết cấu hình electron của nguyên tử các nguyên tố đó.
b) Sắp xếp các nguyên tố trên (trừ H) theo chiều bán kính nguyên tử tăng dần và giải thích.
c) Sắp xếp các nguyên tố trên (trừ H) theo chiều độ âm điện giảm dần và giải thích.
Lời giải
a) Từ công thức của borax là Na2B4O7.10H2O ta xác định được thành phần của borax gồm các nguyên tố sau: Na, B, O, H.
+ Nguyên tố Na nằm ở ô 11, chu kì 3, nhóm IA. Cấu hình electron của nguyên tử Na là 1s2 2s2 2p6 3s1.
+ Nguyên tố B nằm ở ô 5, chu kì 2, nhóm IIIA. Cấu hình electron của nguyên tử B là 1s2 2s22p1.
+ Nguyên tố O nằm ở ô 8, chu kì 2, nhóm VIA. Cấu hình electron của nguyên tử O là 1s2 2s2 2p4.
+ Nguyên tố H nằm ở ô 1, chu kì 1, nhóm IA. Cấu hình electron của nguyên tử H là 1s1.
b) Thứ tự bán kính nguyên tử tăng dần: O < B < Na.
Ta có: O và B thuộc cùng chu kì 2, theo quy luật biến đổi bán kính ta có bán kính O < B.
Na ở chu kì 3, có bán kính nguyên tử lớn hơn so với hai nguyên tử ở chu kì 2.
c) Thứ tự độ âm điện giảm dần: O > B > Na
Ta có: Trong một chu kì, độ âm điện tăng từ trái qua phải (theo chiều tăng của điện tích hạt nhân) nên độ âm điện: B < O và Na < Al.
Trong một nhóm, theo chiều tăng của điện tích hạt nhân (chiều từ trên xuống dưới) độ âm điện giảm nên độ âm điện: Al < B.
Lời giải
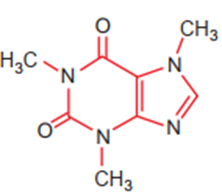
a) Từ công thức cấu tạo của cafein, xác định được các nguyên tố tạo nên cafein là C, N, O, H.
+ Nguyên tố C thuộc ô thứ 6, chu kì 2, nhóm IVA.
+ Nguyên tố N thuộc ô thứ 7, chu kì 2, nhóm VA.
+ Nguyên tố O thuộc ô thứ 8, chu kì 2, nhóm VIA.
+ Nguyên tố H thuộc ô thứ 1, chu kì 1, nhóm IA.
b)
- Các nguyên tố C, N, O cùng thuộc chu kì 2 nên:
+ Tính phi kim tăng dần C < N < O do trong 1 chu kì tính phi kim tăng dần từ trái qua phải.
+ Bán kính nguyên tử giảm C > N > O do trong 1 chu kì bán kính nguyên tử giảm từ trái qua phải.
+ Độ âm điện tăng dần C < N < O do trong 1 chu kì độ âm điện tăng dần từ trái sang phải.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.