Quan sát Hình 4.1 và 4.2, so sánh điểm giống và khác nhau giữa mô hình Rutherford - Bohr với mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử.
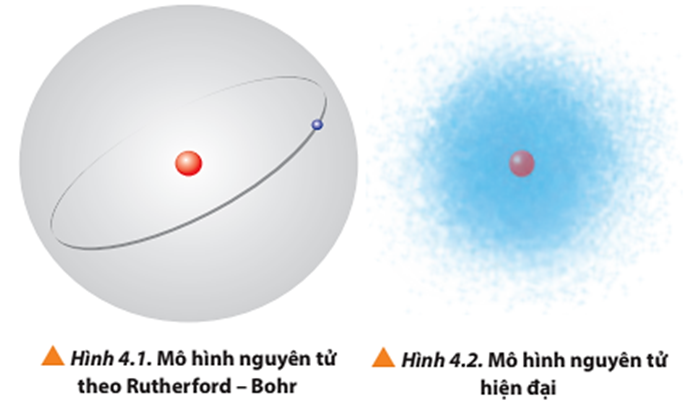
Quan sát Hình 4.1 và 4.2, so sánh điểm giống và khác nhau giữa mô hình Rutherford - Bohr với mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử.

Câu hỏi trong đề: Bài tập Cấu trúc lớp vỏ electron của nguyên tử có đáp án !!
Quảng cáo
Trả lời:
Điểm giống nhau: Nguyên tử gồm hạt nhân mang điện tích dương và vỏ nguyên tử chứa electron mang điện tích âm. Electron chuyển động quanh hạt nhân.
Khác nhau:
- Theo Rutherford – Bohr:
+ Chưa tìm ra hạt neutron.
+ Hạt nhân nằm ở giữa, electron chuyển động quanh hạt nhân trên quỹ đạo đường đi xác định có hình tròn hoặc hình bầu dục.
- Theo mô hình hiện đại:
+ Đã tìm ra hạt neutron.
+ Electron chuyển động hỗn loạn không có quỹ đạo xác định quanh hạt nhân ⇒ Chỉ xác định được khoảng không gian mà electron chuyển động trong đó, khoảng không gian đó gọi là Orbital nguyên tử.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
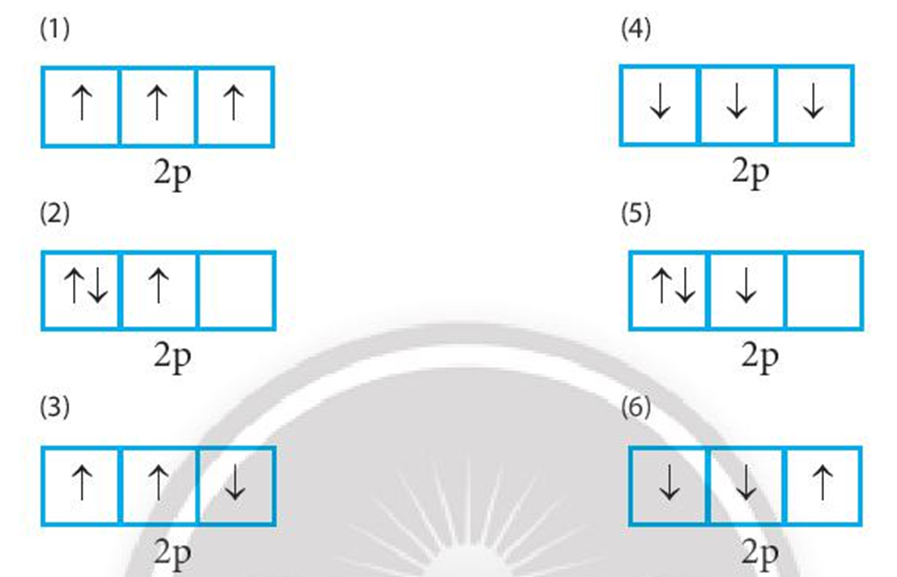
Ở trạng thái cơ bản, nguyên tử của tất cả các nguyên tố trên đều chứa electron độc thân.

Lời giải
Carbon (Z = 6): 1s22s22p2
Từ cấu hình electron ⇒ Nguyên tử carbon có 4 electron lớp ngoài cùng ⇒ Là phi kim.
Sodium (Z = 11): 1s22s22p63s1
Từ cấu hình electron ⇒ Nguyên tử sodium có 1 electron lớp ngoài cùng ⇒ Là kim loại.
Oxygen (Z = 8): 1s22s22p4
Từ cấu hình electron ⇒ Nguyên tử oxygen có 6 electron lớp ngoài cùng ⇒ Là phi kim.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.