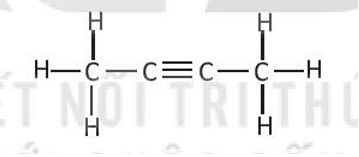
Dùng công thức Lewis để biểu diễn phân tử SO3 sao cho phù hợp với quy tắc octet. Chỉ rõ các liên kết trong phân tử thuộc loại liên kết nào.
Dùng công thức Lewis để biểu diễn phân tử SO3 sao cho phù hợp với quy tắc octet. Chỉ rõ các liên kết trong phân tử thuộc loại liên kết nào.
Câu hỏi trong đề: Giải SBT Hóa học Bài 14. Ôn tập chương 3 có đáp án !!
Quảng cáo
Trả lời:
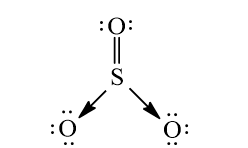
Nguyên tử trung tâm S có 6 electron lớp ngoài cùng và nguyên tử O cũng có 6 electron lớp ngoài cùng. Khi tạo thành phân tử SO3, nguyên tử S và 1 nguyên tử O dùng chung 2 cặp electron để tạo 2 liên kết cộng hóa trị kép phân cực. Để thỏa mãn quy tắc octet, liên kết cộng hóa trị giữa nguyên tử S và 2 nguyên tử O còn lại được thực hiện bằng sự cho – nhận 2 cặp electron của nguyên tử S. Kết quả, trong phân tử SO3, các nguyên tử S và O đều có 8 electron lớp ngoài cùng thỏa mãn quy tắc octet.
Công thức Lewis:
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
A. Tính bão hòa lớp electron ở vỏ nguyên tử.
Liên kết ion khác với liên kết cộng hóa trị là liên kết cộng hóa trị có tính định hướng trong không gian.
Liên kết cộng hóa trị được tạo thành do sự xen phủ các orbital theo trục liên kết (s, px, py, pz).
Lời giải
Đáp án:
A. H2S
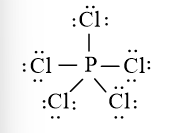
Quy tắc octet không đúng với trường hợp phân tử PCl5 vì xung quanh P có 10 electron liên kết.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.