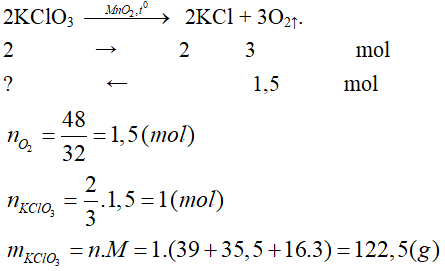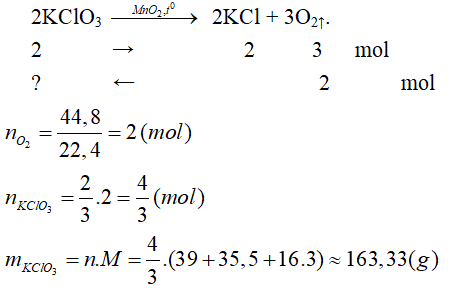Bài 27: Điều chế khí oxi - Phản ứng phân hủy
25 người thi tuần này 4.6 9.9 K lượt thi 6 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 18)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 17)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 16)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 15)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 14)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 13)
Đề kiểm tra giữa học kì 2 Hóa học 8 có đáp án (Mới nhất) (Đề 12)
Đề kiểm tra cuối kì 2 Hóa 8 có đáp án (Mới nhất) (Đề 17)
Danh sách câu hỏi:
Lời giải
Chọn đáp án: b) KClO3. c) KMnO4.
2KClO3 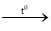
2KMnO4 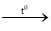
Lời giải
Sự khác nhau về cách điều chế oxi trong phòng thí nghiệm (PTN) và trong công nghiệp (CN).
- Nguyên liệu:
PTN: KClO3 hoặc KMnO4(chất giàu oxi, phản ứng thực hiện nhanh, dễ dàng)
CN: Không khí và nước.
- Sản lượng:
PTN: Thể tích nhỏ dùng cho thí nghiệm.
CN: Sản lượng lớn dùng cho công nghiệp và y tế.
- Giá thành:
PTN: Giá thành cao.
CN: Giá thành hạ vì nguyên liệu là không khí và nước.
Cách điều chế trong CN và PTN cũng khác nhau, trong PTN nhiệt phân KClO3 (hoặc KMnO4) còn trong CN từ hóa lỏng không khí hay điện phân nước
Lời giải
Sự khác nhau giữa phản ứng phân hủy và phản ứng hóa hợp.
Phản ứng hóa hợp là phản ứng hóa học trong đó chỉ có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
Thí dụ:
CaO + CO2 → CaCO3.
2Cu + O2 → 2CuO.
Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
Thí dụ:
2HgO → 2Hg + O2↑
2KClO3 → 2KCl + 3O2
Lời giải
a) Phương trình phản ứng:
b) Phương trình phản ứng:
Lời giải
a) Phương trình hóa học của phản ứng:
CaCO3 → CaO + CO2.
b) Phản ứng nung vôi thuộc loại phản ứng phân hủy vì một chất sinh ra hai chất mới.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.