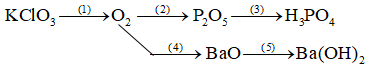Cho 2,4 gam kim loại canxi phản ứng với 68,76 gam nước thu được dung dịch Y và khí hiđro. Dẫn toàn bộ lượng khí hiđro trên qua ống sứ đựng sắt(II) oxit dư, đun nóng.
a) Chất tan trong dung dịch Y là gì? Tính nồng độ phần trăm của dung dịch Y
b) Xác định khối lượng kim loại sắt sinh ra trong ống sứ.
Cho 2,4 gam kim loại canxi phản ứng với 68,76 gam nước thu được dung dịch Y và khí hiđro. Dẫn toàn bộ lượng khí hiđro trên qua ống sứ đựng sắt(II) oxit dư, đun nóng.
a) Chất tan trong dung dịch Y là gì? Tính nồng độ phần trăm của dung dịch Y
b) Xác định khối lượng kim loại sắt sinh ra trong ống sứ.
Câu hỏi trong đề: Đề kiểm tra cuối kì 2 Hóa 8 có đáp án (Mới nhất) !!
Quảng cáo
Trả lời:
a)
Phương trình hoá học: Ca + 2H2O → Ca(OH)2 + H2
Chất tan trong dung dịch Y là Ca(OH)2
Theo phương trình hoá học:
→
= 2,4 + 68,76 – 0,12 = 71,04 (g)
Nông độ phần trăm của dung dịch Y là:
b) Phương trình hoá học:
Theo phương trình hoá học:
→ mFe = 0,06.56 = 3,36(g)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
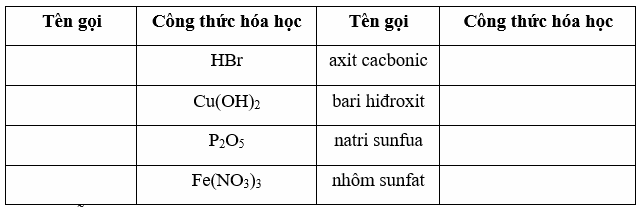
Câu 1
Lời giải
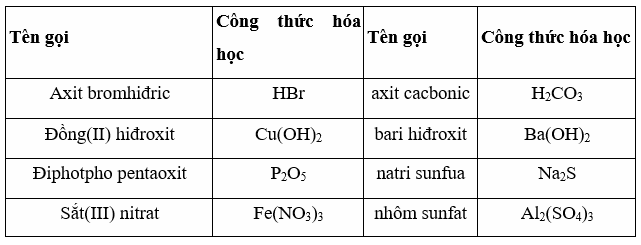
Lời giải
(1)
(2)
(3) P2O5 + 3H2O → 2H3PO4
(4)
(5) BaO + H2O → Ba(OH)2
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.