b. Một loại gas (khí hóa lỏng) chứa hỗn hợp propan (C3H8) và butan (C4H10) với tỉ lệ mol 1 : 2.
Cho biết giá trị ∆rHo298 (lượng chất tham gia phản ứng tính theo mol) của các phản ứng:
C3H8 (k) + O2 (k) → 3CO2 (k) + 4H2O (l)
C4H10 (k) + O2 (k) → 4CO2 (k) + 5H2O (l)
∆rHo298 = -2220 kJ
∆rHo298 = -2874 kJ
Xác định lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn.
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10.000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?
b. Một loại gas (khí hóa lỏng) chứa hỗn hợp propan (C3H8) và butan (C4H10) với tỉ lệ mol 1 : 2.
Cho biết giá trị ∆rHo298 (lượng chất tham gia phản ứng tính theo mol) của các phản ứng:
|
C3H8 (k) + O2 (k) → 3CO2 (k) + 4H2O (l) C4H10 (k) + O2 (k) → 4CO2 (k) + 5H2O (l) |
∆rHo298 = -2220 kJ ∆rHo298 = -2874 kJ |
Xác định lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn.
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10.000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?
Quảng cáo
Trả lời:
b.
-Tính được: = 75 mol, = 150 mol
-Lượng nhiệt: 75.(-2220) + 150.(-2874) = 597600 kJ
-Thời gian sử dụng là: = 47,8 ngày.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
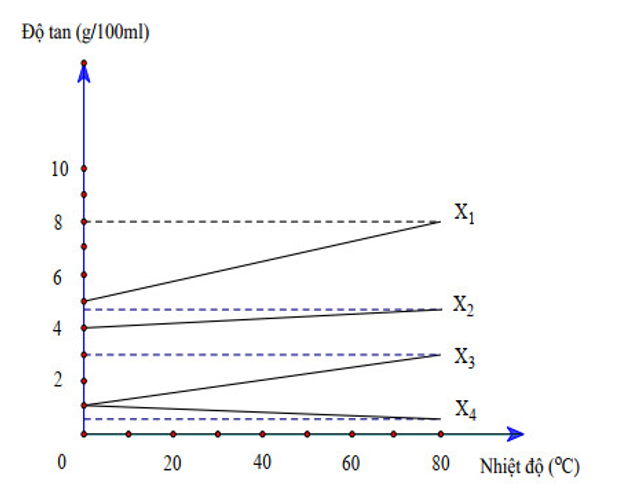
Từ đồ thị ta có thể ước lượng được phần trăm chất tách ra của các chất:
X4 không tách ra
Nên X3 là chất có tỷ lệ tách ra cao nhất
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.