Cho phản ứng đơn giản xảy ra trong bình kín:
3H2(g) + N2 (g) ⟶ 2NH3 (g).
Tốc độ phản ứng thay đổi như thế nào nếu nồng độ H2 không đổi và nồng độ N2 tăng 2 lần?
Cho phản ứng đơn giản xảy ra trong bình kín:
3H2(g) + N2 (g) ⟶ 2NH3 (g).
Tốc độ phản ứng thay đổi như thế nào nếu nồng độ H2 không đổi và nồng độ N2 tăng 2 lần?
A. Tăng 2 lần.
B. Tăng 4 lần.
C. Tăng 8 lần.
D. Tăng 6 lần.
Quảng cáo
Trả lời:
Đáp án đúng là: A
Theo định luật tác dụng khối lượng: \(v = kC_{{H_2}}^3C_{{N_2}}^{}\)
Nếu nồng độ H2 không đổi và nồng độ N2 tăng lên 2 lần, ta có:
\[v' = k\left( {C_{{H_2}}^3} \right)\left( {2.C_{{N_2}}^{}} \right) = 2 \cdot kC_{{H_2}}^3C_{{N_2}}^{} = 2v.\]
Vậy tốc độ phản ứng tăng 2 lần.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
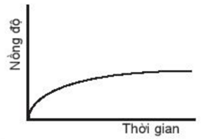
Đáp án đúng là: C
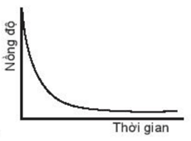
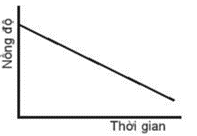
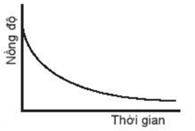
Biểu đồ C cho thấy nồng độ tăng dần theo thời gian, do đó biểu đồ này không biểu diễn sự phụ thuộc nồng độ chất tham gia với thời gian.
Lời giải
Đáp án đúng là: B
Các biện pháp giúp rút ngắn thời gian tiến hành thí nghiệm: (1); (2); (4).
Câu 3
A. chất làm giảm tốc độ phản ứng, nhưng không bị tiêu hao trong phản ứng.
B. chất làm tăng tốc độ phản ứng, nhưng bị tiêu hao trong phản ứng.
C. chất làm tăng tốc độ phản ứng nhưng không bị thay đổi cả lượng và chất sau khi phản ứng kết thúc.
D. chất làm thay đổi tốc độ phản ứng, nhưng bị tiêu hao không nhiều trong phản ứng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. đại lượng đặc trưng cho sự tăng nồng độ của chất phản ứng.
B. đại lượng đặc trưng cho sự thay đổi nồng độ của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
C. đại lượng đặc trưng cho sự thay đổi áp suất của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
D. đại lượng đặc trưng cho sự thay đổi nhiệt độ của chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
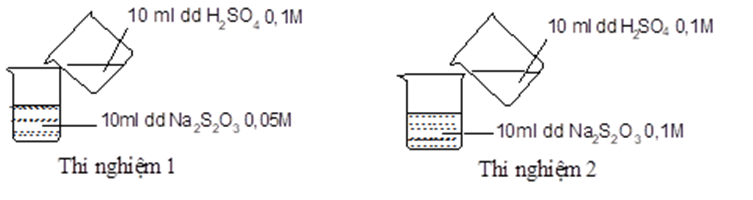
Câu 5
A. Thí nghiệm 1 có kết tủa xuất hiện trước.
B. Thí nghiệm 2 có kết tủa xuất hiện trước.
C. Không xác định được.
D. Không có kết tủa xuất hiện.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. Bắt đầu phản ứng.
B. Khi phản ứng được một nửa lượng chất so với ban đầu.
C. Gần cuối phản ứng.
D. Không xác định được.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. tốc độ phản ứng trung bình.
B. tốc độ tức thời của phản ứng tại một thời điểm.
C. tốc độ phản ứng trung bình tại một thời điểm.
D. tốc độ phản ứng tức thời trong một khoảng thời gian.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.