Cho 2,9825 gam hỗn hợp A gồm: NaX, NaY (X, Y là hai halogen liên tiếp, nguyên tử khối của X nhỏ hơn của Y) vào dung dịch AgNO3 dư. Kết thúc phản ứng thu được 0,7175 gam kết tủa. Xác định hai nguyên tố X, Y.
Quảng cáo
Trả lời:
Đáp án:
Trường hợp 1: X là fluorine, Y là chlorine.
Phương trình hoá học:
NaCl + AgNO3 → NaNO3 + AgCl
Kết tủa là AgCl.
\[{n_{AgCl}} = \frac{{0,7175}}{{108 + 35,5}} = 0,005mol\]
Þ nNaCl = n↓ = 0,005 mol Þ mNaCl = 0,005.58,5 = 0,2925 < mA.
Vậy trường hợp 1 thỏa mãn.
Trường hợp 2: Cả hai muối halogen đều tạo kết tủa
Đặt hai muối NaX và NaY tương ứng với 1 muối là \[Na\overline X \](MNaX < \[{M_{Na\overline X }}\] < MNaY)
Phương trình hoá học:
\[Na\overline X + AgN{O_3} \to NaN{O_3} + Ag\overline {{X_ \downarrow }} \]
\[{n_A} = \frac{{2,9825}}{{23 + {M_{\overline X }}}};{n_ \downarrow } = \frac{{0,7175}}{{108 + {M_{\overline X }}}}\]
Có nA = n↓ nên \[\frac{{2,9825}}{{23 + {M_{\overline X }}}} = \frac{{0,7175}}{{108 + {M_{\overline X }}}} \Leftrightarrow {M_{\overline X }} = - 134,9\]
Vậy trường hợp 2 không thỏa mãn.
Vậy hai halogen là fluorine và chlorine.
Hot: 1000+ Đề thi giữa kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
- Sách - Sổ tay kiến thức trọng tâm Vật lí 10 VietJack - Sách 2025 theo chương trình mới cho 2k9 ( 31.000₫ )
- Trọng tâm Lí, Hóa, Sinh 10 cho cả 3 bộ KNTT, CTST và CD VietJack - Sách 2025 ( 40.000₫ )
- Sách lớp 10 - Combo Trọng tâm Toán, Văn, Anh và Lí, Hóa, Sinh cho cả 3 bộ KNTT, CD, CTST VietJack ( 75.000₫ )
- Sách lớp 11 - Trọng tâm Toán, Lý, Hóa, Sử, Địa lớp 11 3 bộ sách KNTT, CTST, CD VietJack ( 52.000₫ )
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Đáp án: A
\({\Delta _r}H_{298}^o\) = \({\Delta _f}H_{298}^o\)(N2O4) – 2. \({\Delta _f}H_{298}^o\)(NO2)
\({\Delta _r}H_{298}^o\) = 9,16 – 2.33,18 = -57,2 (kJ) < 0.
Phản ứng tỏa nhiệt, N2O4 bền hơn NO2.
Câu 2
Để điều chế khí chlorine (Cl2) trong phòng thí nghiệm, người ta thường cho potassium permanganate (KMnO4) tác dụng với hydrogen chloride (HCl):
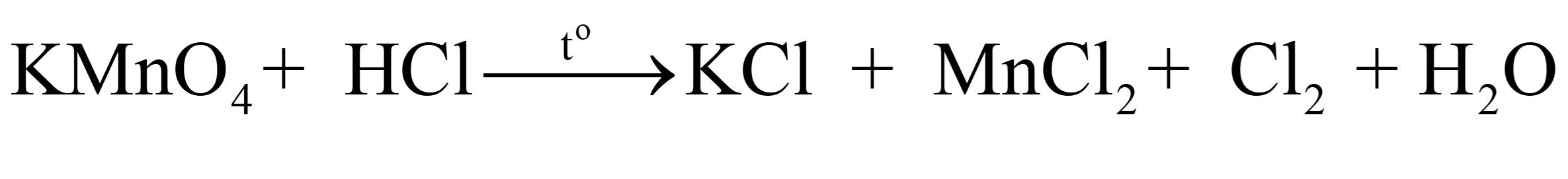
a) Lập phương trình hóa học của phản ứng hóa học trên bằng phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hoá, quá trình oxi hoá, quá trình khử.
b) Giả sử lượng khí chlorine sinh ra phản ứng vừa đủ với dung dịch chứa 9,96 muối KX (X là một nguyên tố halogen) thu được 4,47 gam một muối duy nhất. Xác định công thức phân tử của muối KX.
Để điều chế khí chlorine (Cl2) trong phòng thí nghiệm, người ta thường cho potassium permanganate (KMnO4) tác dụng với hydrogen chloride (HCl):
![]()
a) Lập phương trình hóa học của phản ứng hóa học trên bằng phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hoá, quá trình oxi hoá, quá trình khử.
b) Giả sử lượng khí chlorine sinh ra phản ứng vừa đủ với dung dịch chứa 9,96 muối KX (X là một nguyên tố halogen) thu được 4,47 gam một muối duy nhất. Xác định công thức phân tử của muối KX.
Lời giải
Đáp án:
a) ![]()
Chất khử: HCl.
Chất oxi hoá: KMnO4.
Quá trình khử: \[\mathop {Mn}\limits^{ + 7} + 5e \to \mathop {Mn}\limits^{ + 2} \]
Quá trình oxi hoá: \[2\mathop {Cl}\limits^{ - 1} \to {\mathop {Cl}\limits^0 _2} + 2e\]
Phương trình hoá học được cân bằng:
![]()
b)
Cl2 + 2KX → 2KCl + X2
\[{n_{KX}} = {\rm{ }}{n_{KCl}} = \frac{{4,47}}{{74,5}} = 0,06\,\,(mol)\]
\[{M_{KX}} = \frac{{9,96}}{{0,06}} = 166\]
Vậy MX = 166 – 39 =127 nên KX là KI.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.