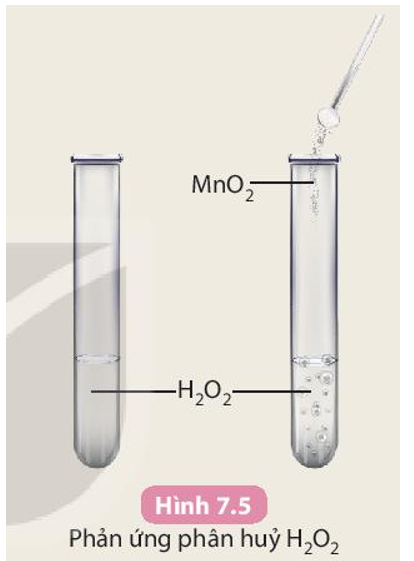
Ảnh hưởng của nồng độ đến tốc độ phản ứng
Chuẩn bị: dung dịch HCl 0,1 M, dung dịch HCl 1 M, 2 đinh sắt giống nhau (khoảng 0,2 g); ống nghiệm.
Tiến hành:
- Cho vào ống nghiệm (1) khoảng 5 mL dung dịch HCl 0,1 M; ống nghiệm (2) khoảng 5 mL dung dịch HCl 1 M.
- Nhẹ nhàng đưa lần lượt 2 đinh sắt vào 2 ống nghiệm và quan sát sự thoát khí.
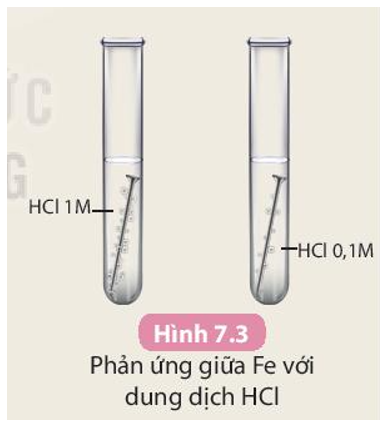
Trả lời câu hỏi:
- Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
- Nồng độ ảnh hưởng đến tốc độ phản ứng như thế nào?
Ảnh hưởng của nồng độ đến tốc độ phản ứng
Chuẩn bị: dung dịch HCl 0,1 M, dung dịch HCl 1 M, 2 đinh sắt giống nhau (khoảng 0,2 g); ống nghiệm.
Tiến hành:
- Cho vào ống nghiệm (1) khoảng 5 mL dung dịch HCl 0,1 M; ống nghiệm (2) khoảng 5 mL dung dịch HCl 1 M.
- Nhẹ nhàng đưa lần lượt 2 đinh sắt vào 2 ống nghiệm và quan sát sự thoát khí.

Trả lời câu hỏi:
- Phản ứng ở ống nghiệm nào xảy ra nhanh hơn?
- Nồng độ ảnh hưởng đến tốc độ phản ứng như thế nào?
Quảng cáo
Trả lời:
- Phản ứng ở ống nghiệm (2) (tức ống nghiệm chứa HCl 1 M) xảy ra nhanh hơn.
- Khi tăng nồng độ chất tham gia phản ứng thì tốc độ phản ứng tăng.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Khi “bảo quản thực phẩm trong tủ lạnh để giữ thực phẩm tươi lâu hơn” là đã tác động vào yếu tố nhiệt độ để làm chậm tốc độ phản ứng.
Lời giải
Phản ứng giữa hydrochloric acid với đá vôi dạng bột xảy ra nhanh hơn so với phản ứng giữa hydrochloric acid với đá vôi dạng viên.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.