Điện phân (với điện cực trơ, màng ngăn) dung dịch chứa x mol CuSO4 và y mol NaCl (x > y) bằng dòng điện một chiều có cường độ 2,68A, sau thời gian t giờ, khối lượng dung dịch Y có khối lượng giảm 20,45 gam so với dung dịch ban đầu. Thêm tiếp Al dư vào Y, thấy thoát ra 3,36 lít khí H2 và dung dịch sau phản ứng chứa 2 chất tan có số mol bằng nhau. Giả thiết hiệu suất điện phân là 100%, các khí sinh ra không tan trong nước và nước không bay hơi trong quá trình điện phân. Giá trị của t gần nhất với giá trị nào sau đây?
Quảng cáo
Trả lời:
nSO42- > nNa+ nên 2 chất tan có số mol bằng nhau là Na2SO4 (0,5y) và Al2(SO4)3 (0,5y)
Bảo toàn S → x = 0,5y + 1,5y (1)
TH1: Cu2+ chưa bị điện phân hết
nH2 = 0,15 → nH+ = 0,3 → nO2 = nH+/4 = 0,075
Anot: nCl2 = 0,5y và nO2 = 0,075
Catot: nCu = 0,5y + 0,15
m giảm = 71.0,5y + 0,075.32 + 64(0,5y + 0,15) = 20,45 (2)
(1)(2) → x = 0,2504; y = 0,1252
→ ne = 2(0,5y + 0,15) = It/F → t = 15310s = 4,25h
TH2: Cu2+ đã bị điện phân hết
nH2 = 0,15 → nAl = y = 0,1
(1) → x = 0,2
Catot: nCu = 0,2 và nH2 = a
Anot: nCl2 = 0,05 và nO2 = b
Bảo toàn electron → 0,2.2 + 2a = 0,05.2 + 4b
m giảm = 0,2.64 + 2a + 0,05.71 + 32b = 20,45
→ a = 17/180; b = 11/90
→ ne = 0,2.2 + 2a = It/F → t = 21204s = 5,9h
Hot: 1000+ Đề thi giữa kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
- 500 Bài tập tổng ôn Hóa học (Form 2025) ( 38.000₫ )
- 1200 câu hỏi lí thuyết Hóa học (Form 2025) ( 38.000₫ )
- Bộ đề thi tốt nghiệp 2025 các môn Toán, Lí, Hóa, Văn, Anh, Sinh, Sử, Địa, KTPL (có đáp án chi tiết) ( 36.000₫ )
- Tổng ôn lớp 12 môn Toán, Lí, Hóa, Văn, Anh, Sinh Sử, Địa, KTPL (Form 2025) ( 36.000₫ )
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Chọn B
Lời giải
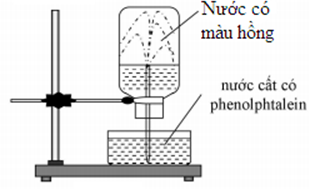
(a) Đúng, NH3 tan tốt làm áp suất trong bình giảm dẫn đến nước bị hút lên.
(b) Sai, tia nước phun mạnh vào bình thủy tinh do áp suất trong bình thấp hơn áp suất không khí.
(c) Sai, nếu dùng quỳ tím thì nước trong bình chuyển màu xanh do NH3 có tính kiềm.
(d) Sai, nhiệt độ càng cao, độ tan chất khí càng giảm.
(e) Sai, thay NH3 bằng HCl thì nước cũng bị hút và phun vào bình nhưng phenolphtalein không đổi màu trong môi trường axit.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.