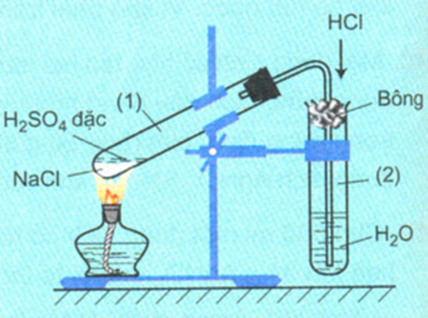
Điện phân dung dịch chứa m gam hỗn hợp gồm NaCl và CuSO4 bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A. Quá trình điện phân diễn ra như sau:
- Sau thời gian t giây, nước đã tham gia điện phân và khí thoát ra ở bình điện phân là 0,1 mol.
- Sau thời gian (t + 2316) giây, khí thoát ra ở bình điện phân là 0,2 mol.
- Sau thời gian 4t giây, khí thoát ra ở bình điện phân là 0,47 mol.
Biết các khí sinh ra không tan trong dung dịch và hiệu suất quá trình điện phân đạt 100%. Giá trị của m là
Câu hỏi trong đề: (2024) Đề minh họa tham khảo BGD môn Hóa có đáp án (Đề 7) !!
Quảng cáo
Trả lời:
Trường hợp 1:
Nếu tại t giây, nước điện phân tạo khí O2
Khi đó, tại thời gian (t + 2316) giây
- Số mol electron tăng thêm = 0,12 mol
- Số mol khí tăng thêm = 0,2 – 0,1 = 0,1 mol
tăng thêm =0.12:4=0,03 Loại
Trường hợp 2:
Nếu tại t giây, nước điện phân tạo khí H2
Tại t giây: n
Xét trong 2316 giây:
Tại 4t giây:
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Khối lượng tinh bột \[ = 2.180.2.0,7.0,7.0,75 = 264,6\] Số mol tinh bột \[ = \frac{{264,6}}{{162}} = \frac{{49}}{{30}}\]
Số mol rượu \[ = 2.\frac{{49}}{{30}} = \frac{{49}}{{15}}\] Khối lượng rượu \[ = \frac{{49}}{{15}}.46 = \frac{{2254}}{{15}}\]
Số lít rượu nguyên chất \[ = \frac{{2254}}{{15}}:0,8 = \frac{{1127}}{6}\]
Số lít dung dịch rượu nấu được \[ = \frac{{1127}}{6}:0,3 \approx 626,1\] Số tiền \[ = \frac{{626,1.20000}}{{{{10}^6}}} = 12,52\] (triệu)
Câu 2
Lời giải
Trước điện phân:
Sau điện phân:
(giờ)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.