Chuẩn độ acid base được sử dụng rất rộng rãi để xác định nồng độ các dung dịch acid hoặc các dung dịch base. Trong phương pháp chuẩn độ acid – base người ta dùng dung dịch kiềm (NaOH hoặc KOH) đã biết chính xác nồng độ làm dung dịch chuẩn để chuẩn độ dung dịch acid hoặc dùng dung dịch acid mạnh 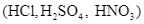 đã biết chính xác nồng độ để chuẩn độ dung dịch base. Trong quá trình chuẩn độ, pH của dung dịch thay đổi liên tục theo lượng dung dịch chuẩn thêm vào.
đã biết chính xác nồng độ để chuẩn độ dung dịch base. Trong quá trình chuẩn độ, pH của dung dịch thay đổi liên tục theo lượng dung dịch chuẩn thêm vào.
Tại điểm tương đương (là thời điểm mà dung dịch chuẩn vừa trung hòa hết dung dịch acid hoặc base cần chuẩn độ) giá trị pH của dung dịch phụ thuộc vào bản chất của acid hoặc base cần chuẩn độ và nồng độ của chúng.
Để nhận ra điểm tương đương của phản ứng chuẩn độ, người ta dùng chất chỉ thị gọi là chất chỉ thị acid - base hay chất chỉ thị pH (màu của chất chỉ thị phụ thuộc vào pH của dung dịch). Với mỗi phản ứng chuẩn độ acid - base người ta chọn chất chỉ thị có khoảng pH đổi màu nằm trong bước nhảy pH (sự thay đổi pH của dung dịch một cách đột ngột xung quanh điểm tương đương). Có thể xác định bước nhảy pH dựa vào việc xác định pH của dung dịch ở thời điểm gần sát (sai số cho phép là ±0,1%) điểm tương đương.
Thí nghiệm: Một sinh viên tiến hành thí nghiệm chuẩn độ như sau:
- Lấy 100 mL dung dịch HCl 0,1 M vào bình tam giác thủy tinh.
- Lấy dung dịch chuẩn NaOH 0,1 M vào burette.
- Mở van khóa của burette để thêm từ từ dung dịch chuẩn NaOH vào bình tam giác thủy tinh. Sinh viên ghi lại quá trình làm thí nghiệm và tính được pH của dung dịch trong quá trình chuẩn độ, kết quả được ghi trong bảng sau:
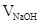
0
10
50
90
99
99,9
100
100,1
101
110
pH
1
1,1
1,48
2,28
3,30
4,30
7,0
9,70
10,7
11,68
Nếu sinh viên sử dụng chất chỉ thị là phenolphthalein thì hiện tượng quan sát được trong bình tam giác thủy tinh tại thời điểm thêm 110 mL dung dịch NaOH là
Chuẩn độ acid base được sử dụng rất rộng rãi để xác định nồng độ các dung dịch acid hoặc các dung dịch base. Trong phương pháp chuẩn độ acid – base người ta dùng dung dịch kiềm (NaOH hoặc KOH) đã biết chính xác nồng độ làm dung dịch chuẩn để chuẩn độ dung dịch acid hoặc dùng dung dịch acid mạnh ![]() đã biết chính xác nồng độ để chuẩn độ dung dịch base. Trong quá trình chuẩn độ, pH của dung dịch thay đổi liên tục theo lượng dung dịch chuẩn thêm vào.
đã biết chính xác nồng độ để chuẩn độ dung dịch base. Trong quá trình chuẩn độ, pH của dung dịch thay đổi liên tục theo lượng dung dịch chuẩn thêm vào.
Tại điểm tương đương (là thời điểm mà dung dịch chuẩn vừa trung hòa hết dung dịch acid hoặc base cần chuẩn độ) giá trị pH của dung dịch phụ thuộc vào bản chất của acid hoặc base cần chuẩn độ và nồng độ của chúng.
Để nhận ra điểm tương đương của phản ứng chuẩn độ, người ta dùng chất chỉ thị gọi là chất chỉ thị acid - base hay chất chỉ thị pH (màu của chất chỉ thị phụ thuộc vào pH của dung dịch). Với mỗi phản ứng chuẩn độ acid - base người ta chọn chất chỉ thị có khoảng pH đổi màu nằm trong bước nhảy pH (sự thay đổi pH của dung dịch một cách đột ngột xung quanh điểm tương đương). Có thể xác định bước nhảy pH dựa vào việc xác định pH của dung dịch ở thời điểm gần sát (sai số cho phép là ±0,1%) điểm tương đương.
Thí nghiệm: Một sinh viên tiến hành thí nghiệm chuẩn độ như sau:
- Lấy 100 mL dung dịch HCl 0,1 M vào bình tam giác thủy tinh.
- Lấy dung dịch chuẩn NaOH 0,1 M vào burette.
- Mở van khóa của burette để thêm từ từ dung dịch chuẩn NaOH vào bình tam giác thủy tinh. Sinh viên ghi lại quá trình làm thí nghiệm và tính được pH của dung dịch trong quá trình chuẩn độ, kết quả được ghi trong bảng sau:
|
|
0 |
10 |
50 |
90 |
99 |
99,9 |
100 |
100,1 |
101 |
110 |
|
|
pH |
1 |
1,1 |
1,48 |
2,28 |
3,30 |
4,30 |
7,0 |
9,70 |
10,7 |
11,68 |
|
B. dung dịch trong bình tam giác thủy tinh có màu xanh.
C. dung dịch trong bình tam giác thủy tinh có màu đen.
Quảng cáo
Trả lời:
Theo bảng số liệu được ghi lại trong thí nghiệm, tại thời điểm thêm 110 mL dung dịch NaOH, dung dịch trong bình tam giác thủy tinh có pH = 11,68 hay có môi trường kiềm. Vậy dung dịch trong bình tam giác thủy tinh có màu hồng.
Chọn A.
Câu hỏi cùng đoạn
Câu 2:
Đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ ở thí nghiệm trên là (đường biểu diễn trên đồ thị đó gọi là đường định phân)
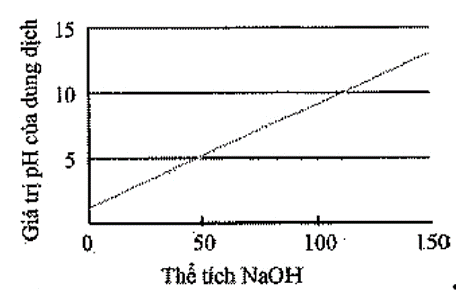
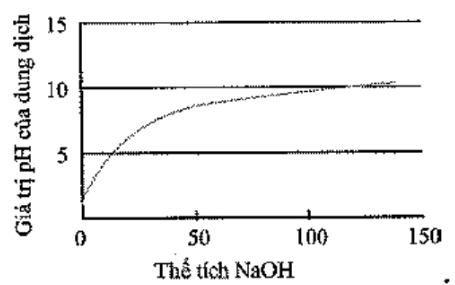
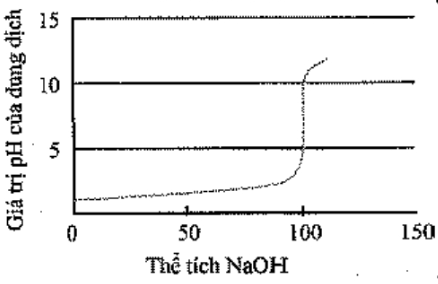
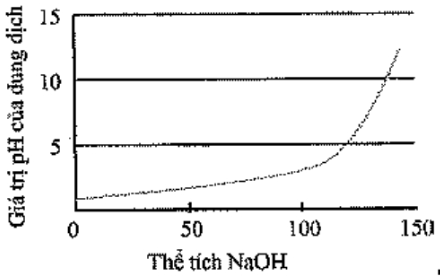
Để vẽ đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ ở thí nghiệm trên ta dựa vào bảng kết quả được ghi trong thí nghiệm trên để vẽ biểu đồ, trong đó trục hoành của biểu đồ ghi thể tích dung dịch NaOH, trục tung ghi giá trị pH của dung dịch. Để vẽ được đường định phân, ta cần tìm các điểm thuộc đường định phân để nối chúng lại với nhau.
Để tìm được điểm trên đường định phân, trên trục hoành tại điểm có giá trị ![]() kẻ đường thẳng a song song với trục tung, trên trục tung tại điểm có giá trị pH = 1,1 kẻ đường thẳng b song song với trục hoành, giao điểm của 2 đường thẳng a và b chính là 1 điểm thuộc đường định phân, các điểm còn lại trên đường định phân học sinh tìm tương tự.
kẻ đường thẳng a song song với trục tung, trên trục tung tại điểm có giá trị pH = 1,1 kẻ đường thẳng b song song với trục hoành, giao điểm của 2 đường thẳng a và b chính là 1 điểm thuộc đường định phân, các điểm còn lại trên đường định phân học sinh tìm tương tự.
Khi đó biểu đồ biểu thị sự biến thiên pH của dung dịch trong quá trình chuẩn độ ở thí nghiệm trên có dạng như hình bên.
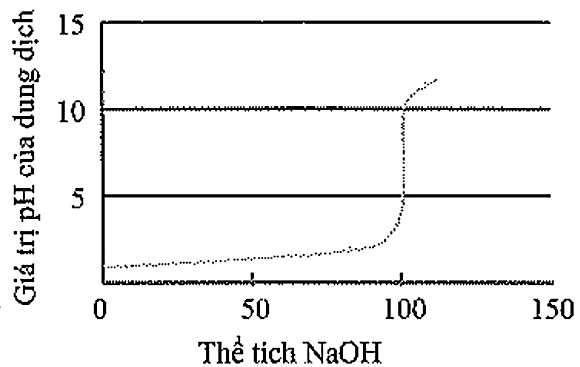
Chọn C.
Câu 3:
Bảng sau đây ghi khoảng pH đổi màu của 3 chất chỉ thị thường được sử dụng nhiều trong chuẩn độ acid – base
Tên chất chỉ thị
Khoảng pH đổi màu
Màu dạng acid – dạng base
Methyl da cam
3,1 - 4,4
Đỏ – Vàng
Methyl đỏ
4,2 - 6,3
Đỏ – Vàng
Phenolphthalein
8,3 - 100
Không màu – Đỏ
Chất chỉ thị nào có thể sử dụng cho quá trình chuẩn độ ở thí nghiệm trên?
Bảng sau đây ghi khoảng pH đổi màu của 3 chất chỉ thị thường được sử dụng nhiều trong chuẩn độ acid – base
|
Tên chất chỉ thị |
Khoảng pH đổi màu |
Màu dạng acid – dạng base |
|
Methyl da cam |
3,1 - 4,4 |
Đỏ – Vàng |
|
Methyl đỏ |
4,2 - 6,3 |
Đỏ – Vàng |
|
Phenolphthalein |
8,3 - 100 |
Không màu – Đỏ |
Chất chỉ thị nào có thể sử dụng cho quá trình chuẩn độ ở thí nghiệm trên?
A. Chỉ sử dụng được methyl da cam.
B. Chỉ sử dụng được methyl đỏ.
C. Chỉ sử dụng được phenolphthalein.
Xung quanh điểm tương đương (thời điểm thêm 100 mL NaOH) có sự thay đổi pH rất đột ngột: Khi thêm 99,9 mL NaOH vào tức là khi đã chuẩn độ 99,9% lượng acid thì pH của dung dịch bằng 4,3. Khi thêm vào 100,1 mL NaOH vào tức là khi đã chuẩn độ quá 0,1% thì pH của dung dịch bằng 9,7 (tức là bước nhảy pH là từ 4,3 đến 9,7). Nếu ta chọn các chất chỉ thị nào có khoảng đổi màu nằm trong khoảng từ 4,3 đến 9,7 để kết thúc chuẩn độ thì sai số không vượt quá 0,1%. Ta thấy trong trường hợp này có thể dùng một trong 3 chất chỉ thị methyl da cam, methyl đỏ và phenolphthalein làm chất chỉ thị.
Chọn D.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Gọi số ngày để hoàn thành công việc nếu người thứ nhất và người thứ hai làm riêng lần lượt là x và y (ngày); ![]() .
.
Suy ra trong 1 ngày người thứ nhất và người thứ hai làm được ![]() và
và ![]() phần công việc.
phần công việc.
Theo giả thiết ta có: 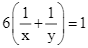 và
và 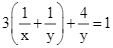 .
.
Suy ra 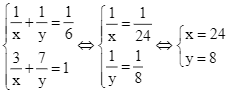 .
.
Vậy nếu làm riêng thì người thứ nhất hoàn thành công việc đó trong 24 ngày. Chọn C.
Câu 2
Lời giải
Gọi giá của chiếc laptop đó là x (triệu đồng) (x > 0).
Tổng số tiền chị Mai phải trả góp trong 2 năm (24 tháng) là: ![]() (triệu đồng).
(triệu đồng).
Theo giả thiết ta có: ![]() .
.
Vậy chị Mai mua chiếc laptop đó với giá là 14 triệu đồng. Chọn C.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















