Trong phòng thí nghiệm, có thể điều chế lượng nhỏ và bằng phương pháp điện phân nước. Một dòng điện 1,04 A đi qua dung dịch sulfuric acid loãng trong 6,00 phút trong một thiết bị điện phân. Tổng số mol và thu được là Giá trị của n là bao nhiêu? (Kết quả làm tròn đến hàng phần trăm).
Cho biết số mol electron đi qua hệ tính theo công thức với I là cường độ dòng điện (A), t là thời gian (giây), là số Faraday.
Trong phòng thí nghiệm, có thể điều chế lượng nhỏ và bằng phương pháp điện phân nước. Một dòng điện 1,04 A đi qua dung dịch sulfuric acid loãng trong 6,00 phút trong một thiết bị điện phân. Tổng số mol và thu được là Giá trị của n là bao nhiêu? (Kết quả làm tròn đến hàng phần trăm).
Cho biết số mol electron đi qua hệ tính theo công thức với I là cường độ dòng điện (A), t là thời gian (giây), là số Faraday.
Câu hỏi trong đề: Bộ 3 đề thi giữa kì 2 Hóa 12 Cánh diều có đáp án !!
Quảng cáo
Trả lời:
Đáp án: 2,91
Sử dụng công thức tính số mol electron:
Có thể coi tạo thành theo quá trình ở cực âm.
tạo thành từ quá trình ở cực dương.
Vậy, tổng số mol và thu được là:
Vậy n = 2,91.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
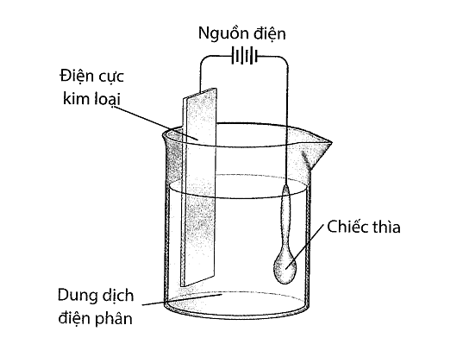
a) Sai. Bạc là kim loại hoạt động hóa học kém.
b) Đúng. Dung dịch điện phân là muối bạc tan tốt trong nước.
c) Đúng. Điện cực kim loại được làm bằng bạc.
d) Đúng. Chiếc thìa được nối với cực âm của nguồn điện.
Câu 2
A. Vỏ tàu bị gì chủ yếu do xảy ra ăn mòn điện hoá học.
B. Để chống sự ăn mòn vỏ tàu người ta thường phủ kín vỏ tàu bằng một lớp sơn.
C. Vỏ tàu bị ăn mòn là do sắt tác dụng với NaCl trong nước biển.
Lời giải
Đáp án đúng là: C
Vỏ tàu bị gì chủ yếu do xảy ra ăn mòn điện hoá học. Thép có thành phần là sắt và carbon, cùng tiếp xúc với nước biển đã tạo nên vô số pin rất nhỏ mà sắt là cathode và carbon là anode.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. ở áp suất cao, khí CO2 có thể đẩy ra khỏi muối NaCl tạo thành NaHCO3.
B. phản ứng oxi hoá - khử xảy ra trong dung dịch.
C. NaHCO3 có độ tan kém trong dung dịch phản ứng, dễ dàng kết tinh.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.