Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Điện phân dung dịch CuCl2 trong 1 giờ với dòng điện 5A. Sau điện phân, dung dịch còn CuCl2 dư. Khối lượng Cu đã sinh ra tại cathode của bình điện phân là bao nhiêu gam? (Cho Cu = 64).
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Điện phân dung dịch CuCl2 trong 1 giờ với dòng điện 5A. Sau điện phân, dung dịch còn CuCl2 dư. Khối lượng Cu đã sinh ra tại cathode của bình điện phân là bao nhiêu gam? (Cho Cu = 64).
Quảng cáo
Trả lời:
Hướng dẫn giải:
Đáp án đúng là: 5,97.
Quá trình oxi hóa ở anode: Cu → Cu2+ + 2e
Số mol electron: ne = 2.nCu
Điện lượng q = ne.F = 2.nCu.F
\[{\rm{I = }}\frac{{\rm{q}}}{{\rm{t}}}{\rm{ }} \Rightarrow {\rm{q = I}}{\rm{.t }} \Leftrightarrow 2{n_{Cu}}F = 5.3600 \Leftrightarrow 2.64.{m_{{\bf{Cu}}}}.F = 5.3600\]
\({{\rm{m}}_{{\rm{Cu}}}} = \frac{{{\rm{64}}{\rm{.5}}{\rm{.3600}}}}{{{\rm{2}}{\rm{.96500}}}} = 5,97g.\)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hướng dẫn giải
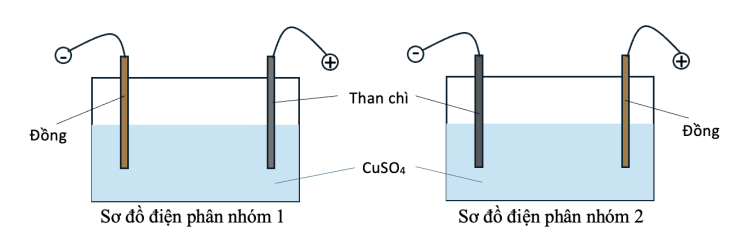
a. Đúng. Cu → Cu2+ + 2e
b. Đúng. Tại cathode cả 2 nhóm: Cu2+ + 2e → Cu.
c. Đúng. Tại anode nhóm 1: 2H2O → 4H+ + O2 + 4e. Do có H+ sinh ra nên pH của dung dịch điện phân giảm dần.
d. Đúng.
Lời giải
Hướng dẫn giải
a. Sai. Vì \({O_2}\)sinh ra có thể phản ứng với C ở điện cực tạo thành
b. Sai. \({{\rm{A}}_{{\rm{tt}}}} = \frac{{{{5.10}^3}.96485}}{{{{9.3,6.10}^6}.95\% }} \approx 15,67{\rm{kWh}}{\rm{.}}\)
c. Đúng. Tại cathode xảy ra quá trình khử cation \[A{l^{3 + }}.\]
d. Đúng. Cryolite làm hạ nhiệt độ nóng chảy của \[A{l_2}{O_3},\]do đó giúp tiết kiệm năng lượng tiêu thụ.\(CO,\,C{O_2}.\)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. graphite.
B. platinum.
C. thép.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. 2AlF3 → 2Al + 3F2.
B. 2NaF → Na + F2.
C. 2H2O → 2H2 + O.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. 2Al2O3 → 4Al + 3O2.
B. 2Al + Cr2O3 → Al2O3 + 2Cr.
C. Zn + CuSO4 → ZnSO4 + Cu.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
![Do \[A{l_2}{O_3}\] có nhiệt độ nóng chảy rất cao \[\left( {2050^\circ C} \right)\] nên \[A{l_2}{O_3}\]được trộn cùng với cryolite \[\left( {N{a_3}Al{F_6}} \right)\] để tạo thành hỗn hợp nóng chảy ở gần \[1000^\circ C.\] Giải pháp này giúp tiết kiệm nhiều năng lượng, đồng thời tạo ra chất lỏng vừa có tính dẫn điện tốt, vừa nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới đây: Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (khoảng 5 V) và cường độ dòng điện 100 – 300 kA. Cho biết: Năng lượng điện tiêu thụ theo lí thuyết: \({{\rm{A}}_{{\rm{lt}}}} = \frac{{{\rm{U}}{\rm{.}}{{\rm{m}}_{{\rm{Al}}}}{\rm{.F}}}}{{{{9.3,6.10}^6}}}{\rm{(kWh) }}\) Trong đó: • mAl: khối lượng Al được điều chế (gam); • F: hằng số Faraday, \[F = 96485{\rm{ }}Cmo{l^{ - 1}};\] • U: hiệu điện thế áp đặt vào hai cực của bình điện phân (V). Hiệu suất tiêu thụ điện năng là 95%. a. Ở anode chỉ có khí \[{O_2}\] thoát ra. b. Năng lượng điện tiêu thụ thực tế để sản xuất được 1 kg Al là 15 kWh. c. Tại cathode xảy ra quá trình khử cation \[A{l^{3 + }}.\] d. Cryolite làm hạ nhiệt độ nóng chảy của \[A{l_2}{O_3},\]do đó giúp tiết kiệm năng lượng tiêu thụ. (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2025/07/blobid0-1752416725.png)