-
Cho biết phản ứng sau có 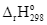 > 0 và diễn ra ngay ở nhiệt độ phòng:
> 0 và diễn ra ngay ở nhiệt độ phòng:
2NH4NO3(s) + Ba(OH)2.8H2O(s)  2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
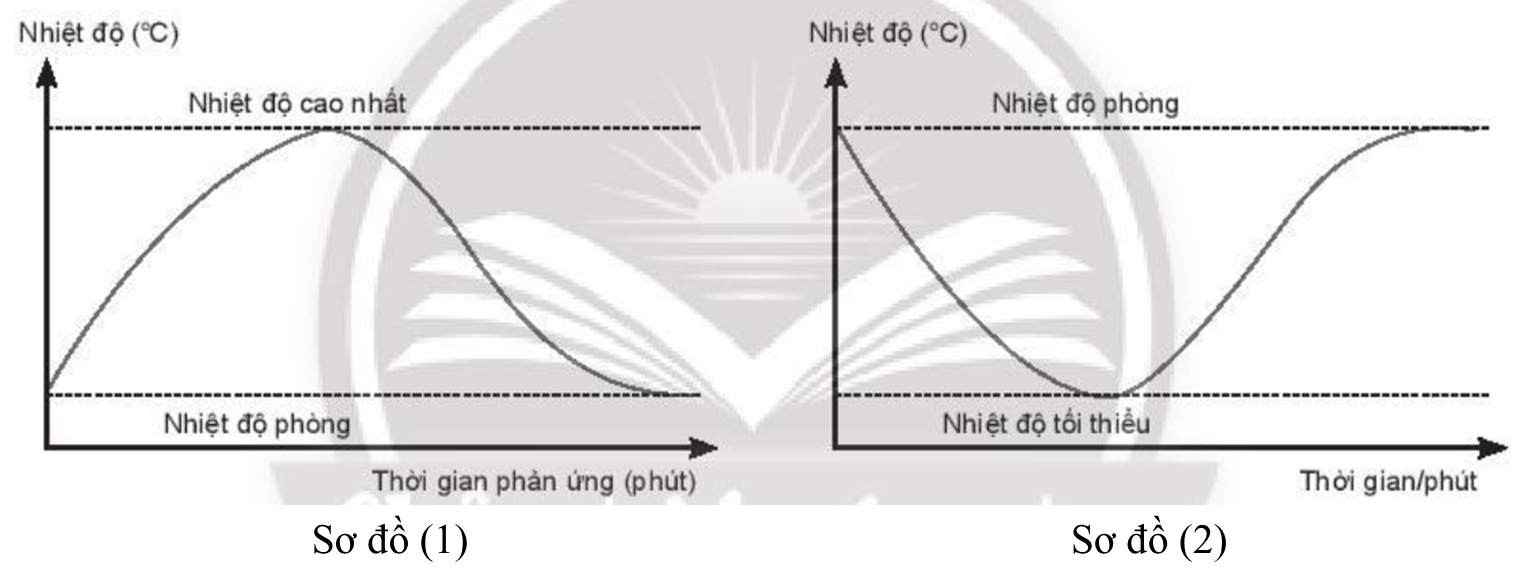
Khi trộn đều một lượng ammonium nitrate (NH4NO3) rắn với một lượng barium hydroxide ngậm nước (Ba(OH)2.8H2O) ở nhiệt độ phòng thì nhiệt độ của hỗn hợp sẽ tăng hay giảm? Giải thích.
-
Cho biết phản ứng sau có
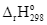 > 0 và diễn ra ngay ở nhiệt độ phòng:
> 0 và diễn ra ngay ở nhiệt độ phòng:
2NH4NO3(s) + Ba(OH)2.8H2O(s) ![]() 2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
Khi trộn đều một lượng ammonium nitrate (NH4NO3) rắn với một lượng barium hydroxide ngậm nước (Ba(OH)2.8H2O) ở nhiệt độ phòng thì nhiệt độ của hỗn hợp sẽ tăng hay giảm? Giải thích.
Quảng cáo
Trả lời:
Ở nhiệt độ phòng thì nhiệt độ của hỗn hợp tăng lên do phản ứng này là phản ứng thu nhiệt.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
a) Nước hóa rắn: quá trình tỏa nhiệt.
b) Sự tiêu hóa thức ăn: quá trình thu nhiệt.
c) Quá trình chạy của con người: quá trình tỏa nhiệt.
d) Khí CH4 đốt ở trong lò: quá trình tỏa nhiệt.
e) Hòa tan KBr vào nước làm cho nước trở nên lạnh: quá trình thu nhiệt.
g) Sulfuric acid đặc khi thêm vào nước làm cho nước nóng lên: quá trình tỏa nhiệt.
Lời giải
(a) Phản ứng (1) là phản ứng thu nhiệt.
(b) Nhiệt tạo thành chuẩn của H2O(g) là –241,8 kJ/mol.
(c) Biến thiên enthalpy chuẩn của phản ứng 2H2(g) + O2(g) ![]() 2H2O(g) là –483,6 kJ.
2H2O(g) là –483,6 kJ.
(d) Biến thiên enthalpy chuẩn của phản ứng (1) là 241,8 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.