Cho biết năng lượng liên kết của Cl2 và N2 như bảng dưới:
| Liên kết | Cl - Cl | N ≡ N |
| E (kJ/mol) | 243 | 945 |
Giải thích vì sao độ âm điện của nitrogen là 3,04 xấp xỉ với độ âm điện của chlorine là 3,16 nhưng ở điều kiện thường, nitrogen kém hoạt động hơn nhiều so với chlorine. Từ đó hãy so sánh khả năng phản ứng của Cl2 và N2 khi cho lần lượt các khí này tác dụng với H2?
Quảng cáo
Trả lời:
Tuy có độ âm điện xấp xỉ nhau nhưng phân tử nitrogen có liên kết ba (N ≡ N) và có năng lượng liên kết (945 kJ/ mol) lớn hơn nhiều so với phân tử chlorine chỉ có liên kết đơn (Cl – Cl) có năng lượng liên kết là 243 kJ/mol, dẫn đến phải tiêu tốn năng lượng nhiều hơn để phá vỡ liên kết trong phân tử nitrogen so với trong phân tử chlorine. Vì vậy ở điều kiện thường, nitrogen kém hoạt động hơn nhiều so với chlorine.
Vậy khả năng phản ứng của Cl2 là lớn hơn nhiều so với N2 khi cho các chất này tác dụng lần lượt với H2.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
X2O3.
XO2.
XO.
X2O5.
Lời giải
Đáp án đúng là D
Lời giải
GĐ1: Tạo thành các ion Na+ và F-
Sự tạo thành ion Na+:
Na Na+ + 1e
[Ne]3s1 [Ne]
Sự tạo thành ion F-:
F + 1e F-
1s22s22p5 1s22s22p6
GĐ2: Ion Na+ và F- hút nhau bằng lực hút tĩnh tiện tạo sodium fluoride (NaF)
Na+ + F- NaF
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Cộng hóa trị phân cực.
Không xác định được bản chất liên kết.
Cộng hóa trị không phân cực.
Liên kết Ion.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















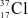 là
là