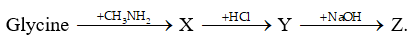Ammonia có nhiều ứng dụng quan trọng như sản xuất phân đạm, nitric acid, làm dung môi. Hiện nay người ta sản xuất ammonia bằng cách chuyển hoá có xúc tác một hỗn hợp gồm không khí, hơi nước và khí methane (thành phần chính của khí thiên nhiên) theo quy trình Haber.
Phản ứng điều chế (1)
Phản ứng loại để thu (2)
Phản ứng tổng hợp
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2). Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane là \(100\% \). Biết \(80\% \) lương nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành \(\left( {{\Delta _f}{\rm{H}}_{298}^0} \right)\) của các chất ở điều kiện chuẩn được cho trong bảng sau:
|
Chất |
\({\rm{C}}{{\rm{H}}_4}\left( {{\rm{\;g}}} \right)\) |
\({\rm{C}}{{\rm{O}}_2}\left( {{\rm{\;g}}} \right)\) |
\({{\rm{H}}_2}{\rm{O}}\left( {\rm{g}} \right)\) |
|
\(\left( {{\rm{\Delta f}}{{\rm{H}}_{298}}{\;^0}\left( {{\rm{\;kJ\;mo}}{{\rm{l}}^{ - 1}}} \right)} \right.\) |
\( - 74,6\) |
\( - 393,5\) |
Để sản xuất được 0,36 tấn khí hydrogen trong giai đoạn trên cần dùng m tấn khí methane. Giá trị của m là?
(Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)
Quảng cáo
Trả lời:
Đáp án:
Đáp án: 0,9
Ta có: \(\left\{ \begin{array}{l}{\Delta _{\rm{f}}}{\rm{H}}_{298}^0(1) = 164,7{\rm{kJ}}\\{\Delta _{\rm{f}}}{\rm{H}}_{298}^0(2) = - 802,5\,\,{\rm{kJ }}\end{array} \right.\)
\({\rm{X\'e t }}(1)\,\,\,\,{{\rm{n}}_{{{\rm{H}}_2}}} = 0,{18.10^6} \Rightarrow {{\rm{n}}_{{\rm{C}}{{\rm{H}}_4}}}(1) = 0,{045.10^6}\,mol\)
Lượng nhiệt cần dùng cho phản ứng (1) là \(0,045.164,{7.10^6} = 7,{4115.10^6}\;{\rm{kJ}}\)
Xét (2): \({{\rm{n}}_{{\rm{C}}{{\rm{H}}_4}}} = {\rm{x}}\) (Mol)
Lượng nhiệt tạo ra ở phản ứng (2) là 802,5x
Lượng nhiệt tạo ra ở phản ứng (2) cung cấp cho phản ứng (1) là 802,5x.80/100
\( \Rightarrow 7,{4115.10^6} = 802,5x \cdot \frac{{80}}{{100}} \Rightarrow x = 0,{01154.10^6}\)
Vậy\(m = 16.0,{0565.10^6} = 0,905\) tấn
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
Đáp án: 97
X: H2NCH2COOH3NCH3
Y: ClH3NCH2COOH3NCH3
Z: H2NCH2COONa (M=97)
Lời giải
Phần trăm năng lượng giải phóng từ sự oxi hóa hoàn toàn lượng glucose bài so với nhu cầu năng lượng trung bình 2000 cal/ngày của một người trưởng thành = \(\frac{{\frac{{300}}{{162}} \times \frac{{80}}{{100}} \times \frac{{60}}{{100}} \times 2880}}{{2000 \times 4184 \times {{10}^{ - 3}}}} \times 100\)= 30,6%
Chọn C
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.