Cho các phương trình nhiệt hóa học của các phản ứng sau:
(1) 3Fe(s) + 4H2O(l) Fe3O4(s) + 4H2(g) = +26,32 kJ
(2) N2(g) + O2(g) 2NO(g) = +179,20 kJ
(3) Na(s) + 2H2O(l) NaOH(aq) + H2(g) = ‒ 367,50 kJ
(4) 2ZnS(s) + 3O2(g) 2ZnO(s) + 2SO2(g) = ‒285,66 kJ
(5) ZnSO4(s) ZnO(s) + SO3(g) ; = + 235,21 kJ
Có bao nhiêu phản ứng thuộc loại phản ứng tỏa nhiệt?
Quảng cáo
Trả lời:
Đáp án:
Đáp án đúng là: 2
Giải thích:
Các phản ứng (3) và (4) là phản ứng tỏa nhiệt do có < 0.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
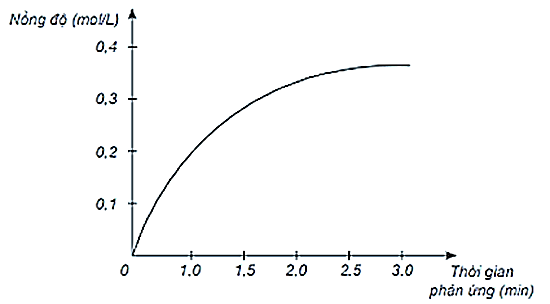
a. Đồ thị mô tả sự thay đổi nồng độ theo thời gian của H2.
b. Đồ thị mô tả sự thay đổi nồng độ theo thời gian của Cl2.
c. Biểu thức tốc độ trung bình của phản ứng là .
d. Phản ứng trên có thể xảy ra ngay trong bóng tối.
Lời giải
a. Sai. Đồ thị mô tả sự thay đổi nồng độ theo thời gian của HCl do nồng độ tăng dần theo thời gian.
b. Sai. Đồ thị mô tả sự thay đổi nồng độ theo thời gian của HCl do nồng độ tăng dần theo thời gian.
c. Đúng.
d. Sai. Phản ứng trên không xảy ra trong bóng tối.
Câu 2
Fe + dung dịch HCl 0,3 M.
Fe + dung dịch HCl 0,5 M.
Fe + dung dịch HCl 0,1 M.
Fe + dung dịch HCl 0,2 M.
Lời giải
Đáp án đúng là: B
Nồng độ các chất tham gia phản ứng càng lớn thì tốc độ phản ứng càng lớn.
Như vậy cặp Fe + dung dịch HCl 0,5 M có tốc độ phản ứng là lớn nhất.
Câu 3
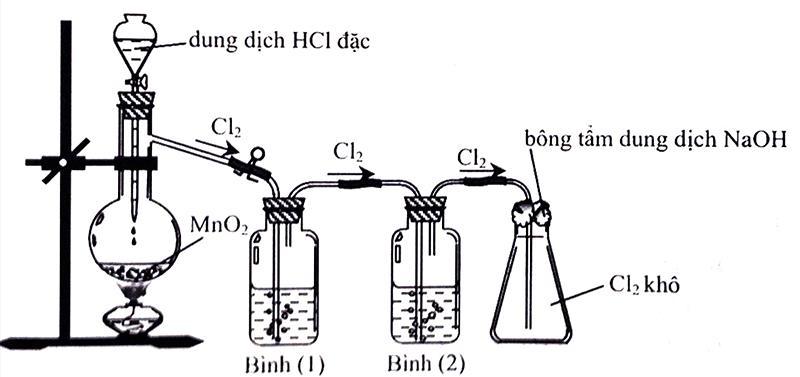
a. Để thu được khí chlorine khô thì bình (1) và bình (2) lần lượt đựng dung dịch NaCl bão hòa và dung dịch H2SO4 đặc.
b. Bông tẩm dung dịch NaOH dùng để ngăn không cho khí chlorine thoát ra ngoài.
c. Có thể thay acid HCl đặc bằng acid H2SO4 đặc.
d. Có thể thu khí chlorine bằng phương pháp đẩy nước.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.