Năng lượng tự do Gibbs (G) là năng lượng của phản ứng hóa học và có thể thực hiện công có ích. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng được tính theo công thức sau: . T là nhiệt độ (K).
Trong đó: và lần lượt là biến thiên enthapy và entropy của phản ứng. Phản ứng tỏa nhiệt thì có giá trị âm còn phản ứng thu nhiệt thì có giá trị dương. Dấu của được dùng để dự đoán chiều hướng xảy ra của một phản ứng hóa học. Nếu âm thì phản ứng tự xảy ra, còn nếu dương thì phản ứng không tự xảy ra.
Năng lượng tự do Gibbs (G) là năng lượng của phản ứng hóa học và có thể thực hiện công có ích. Ở nhiệt độ và áp suất không đổi (p = 1 bar), biến thiên năng lượng tự do của phản ứng được tính theo công thức sau: . T là nhiệt độ (K).
Trong đó: và lần lượt là biến thiên enthapy và entropy của phản ứng. Phản ứng tỏa nhiệt thì có giá trị âm còn phản ứng thu nhiệt thì có giá trị dương. Dấu của được dùng để dự đoán chiều hướng xảy ra của một phản ứng hóa học. Nếu âm thì phản ứng tự xảy ra, còn nếu dương thì phản ứng không tự xảy ra.
Để một phản ứng không tự xảy ra ở mọi nhiệt độ thì
A. > 0 và
B. < 0 và
C. > 0 và
Quảng cáo
Trả lời:
Dấu của được dùng để dự đoán chiều hướng xảy ra của một phản ứng hóa học. Nếu âm thì phản ứng tự xảy ra, còn nếu dương thì phản ứng không tự xảy ra.
trong đó T là nhiệt độ (K). Vậy để > 0 (hay luôn dương) thì > 0 và
Chọn A.
Câu hỏi cùng đoạn
Câu 2:
Một phản ứng hóa học < 0, > 0 và < 0. Phát biểu nào sau đây đúng?
Dựa trên thông tin đoạn văn: “Phản ứng tỏa nhiệt thì có giá trị âm” và “Nếu âm thì phản ứng tự xảy ra”.
Lại có để luôn âm thì < 0 và
Chọn A.
Câu 3:
Một phản ứng hóa học có = 119 kJ và = 263 J/K. Ở nhiệt độ nào sau đây thì phản ứng trên tự xảy ra?
A. 200K.
B. 382K.
C. 363K.
D. 500K.
Phản ứng tự xảy ra khi < 0.
Hay ⇔ T > 452,47K.
Chọn D.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Nước Javel được tạo thành trong bể điện phân.
Dung dịch sau điện phân có thành phần chính là NaCl.
Kim loại sodium thu được ở anode và khí chlorine thu được ở cathode.
Sản phẩm cơ bản của công nghiệp chlorine - kiềm là sodium hydroxide, chlorine và hydrogen.
Lời giải
- Phát biểu A sai do điện phân có màng ngăn.
- Phát biểu B sai do dung dịch sau điện phân có thành phần chính là NaOH.
- Phát biểu C sai do điện phân dung dịch NaCl nên không thu được kim loại Na, ngoài ra khí khí chlorine thu được ở anode.
Chọn D.
Câu 2
Kết tinh.
Nhiệt luyện.
Thuỷ luyện.
Chiết.
Lời giải
Sắt được tạo ra trong quá trình sản xuất gang bằng phương pháp nhiệt luyện.
Phương trình hóa học minh họa:
Chọn B.
Câu 3
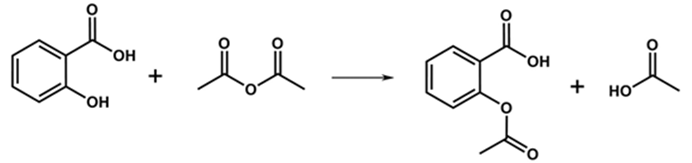
Phản ứng tổng hợp aspirin là phản ứng ester hóa.
Sử dụng phương pháp chiết để tách aspirin ra khỏi hỗn hợp sau phản ứng.
1 mol aspirin tác dụng tối đa với 3 mol NaOH trong dung dịch.
Để tổng hợp aspirin đủ sản xuất 1 triệu viên “aspirin 81” cần dùng ít nhất 621 gam salicylic acid.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Trong phòng thí nghiệm, benzoic acid được điều chế từ toluene theo sơ đồ gồm hai giai đoạn được đánh số (1) và (2) như sau:
Trong một thí nghiệm tổng hợp benzoic acid theo sơ đồ trên, từ 2,0 mL toluene (khối lượng riêng bằng 0,867 g. mL⁻¹) thu được 1,40 gam benzoic acid. Biết và HCl được lấy dư. Hiệu suất của quá trình tổng hợp benzoic acid từ toluene là h%.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
| Liên kết | O–H (alcohol) | O–H
(carboxylic acid) | C=O
(ester, carboxylic acid) |
| Số sóng | 3650–3200 | 3300–2500 | 1780–1650 |
Cho các phát biểu sau:
(a). Giá trị của h là 60,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.)
(b). Trong phản ứng với KMnO4 (aq) ở giai đoạn (1), toluene đóng vai trò là chất oxi hóa.
(c). Trên phổ hồng ngoại của benzoic acid, tín hiệu (peak) ở đặc trưng cho liên kết O–H.
(d). Trong phản ứng ở giai đoạn (2), anion là một base theo thuyết Brønsted – Lowry.
Số phát biểu đúng là
4.
3.
2.
1.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
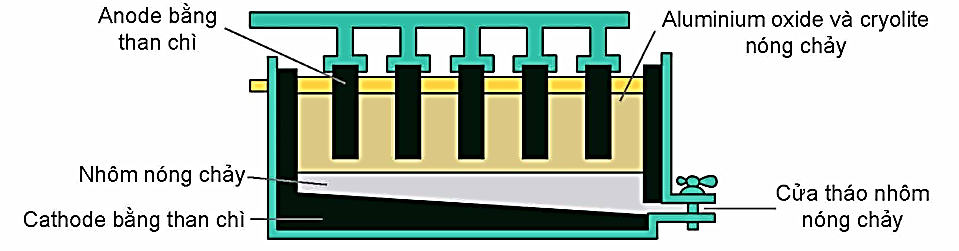
Ở anode không chỉ có khí thoát ra mà còn có thể có cả khí khác.
Năng lượng điện tiêu thụ thực tế để sản xuất được 1 kg Al là 15 kWh.
Tại cathode xảy ra quá trình khử cation
Cryolite làm hạ nhiệt độ nóng chảy của do đó giúp tiết kiệm năng lượng tiêu thụ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.