Một bình kín có thể tích \[2{\rm{ }}lít\] chứa khí oxygen ở \[20\,^\circ C\] dưới áp suất \[1{\rm{ }}atm.\] Sau đó, bình được chuyển đến một nơi có nhiệt độ \[37\,^\circ C.\]
Sau khi chuyển đến chỗ mới, bình xuất hiện một lỗ rò nhỏ. Khối lượng khí thoát ra khỏi bình là bao nhiêu gam? Biết áp suất khí quyển nơi đặt bình là 1 atm và khối lượng mol của oxygen là 32 gam/mol (viết kết quả ở dạng thập phân, làm tròn đến hai chữ số sau dấu phẩy)?
Câu hỏi trong đề: Đề ôn thi Tốt nghiệp THPT Vật lý có đáp án - Đề số 28 !!
Quảng cáo
Trả lời:
Trả lời: 0,15
Khối lượng khí ban đầu: \({m_0} = \frac{{M.p.V}}{{R.{T_1}}}\)
Khối lượng khí sau khi rò lỗ nhỏ: \(m = \frac{{M.p.V}}{{R.{T_2}}}\)
Khối lượng khí thoát ra: \(\Delta m = {m_0} - m = \frac{{M.p.V}}{{R.{T_1}}} - \frac{{M.p.V}}{{R{T_2}}} = 0,146\)g
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Sóng âm.
Sóng hồng ngoại.
Sóng ánh sáng.
Sóng Wi-Fi.
Lời giải
Chọn A
Sóng âm là sóng cơ.
Các sóng còn lại là sóng điện từ là sự lan truyền của điện từ trường trong không gian.
Câu 2
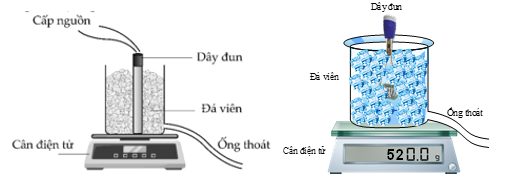
a. Việc đọc số liệu trên cân điện tử phải được thực hiện sau khi tắt nguồn điện.
b. Khối lượng nước đá đã tan trong thời gian đun là \(0,172\,kg.\)
c. Nhiệt lượng cần thiết để làm tan nước đá là \(57600\,J.\)
d. Nhiệt nóng chảy riêng của nước đá là \(3,35 \cdot {10^5}\,J/kg.\)
Lời giải
a) Việc đọc số liệu trên cân điện tử phải được thực hiện sau khi tắt nguồn điện cung cấp cho nước đá.
Chọn ĐÚNG.
b) Khối lượng nước đá đã tan trong thời gian đun là số chỉ của cân điện tử bị giảm đi là \(0,172\,kg.\)
Chọn ĐÚNG.
c) Nhiệt lượng cần thiết để làm tan nước đá là \(Q = P \cdot t = 480 \cdot 120 = 57600\,J\)
Chọn ĐÚNG.
d) Nhiệt nóng chảy riêng của nước đá là \(\lambda = \frac{Q}{m} = \frac{{57600}}{{0,172}} = 3,35 \cdot {10^5}\,J/kg.\)
Chọn ĐÚNG.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
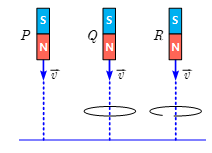
P và R rơi xuống chạm đất cùng lúc, sau đó là Q.
P và Q rơi xuống chạm đất cùng lúc, sau đó là R.
P rơi xuống chạm đất trước, sau đó là Q, R chạm đất cuối cùng.
Cả ba nam châm chạm đất cùng lúc.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
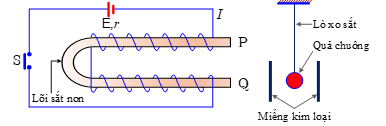
a. Khi ấn công tắc S, lõi sắt non trở thành một nam châm vĩnh cửu với đầu Q là cực bắc, còn đầu P là cực nam.
b. Nếu thay lõi sắt non bằng lõi thép thì sẽ chỉ nghe thấy một tiếng "ding".
c. Nếu thay thanh lò xo sắt thành lò xo đồng thì chuông vẫn sẽ hoạt động bình thường.
d. Nếu đảo hai cực của nguồn điện thì chuông sẽ không hoạt động.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.