Quặng argentite (sau khi đã tuyển quặng) có hàm lượng Ag2S là 86,8% (còn lại là tạp chất trơ). Từ loại quặng này người ta tách lấy kim loại Ag theo các bước sau:
- Bước 1: Xử lí quặng này với dung dịch NaCN bằng phương pháp nghiền ướt xảy ra phản ứng sau:
(1) Ag2S + 4NaCN → 2Na[Ag(CN)2] + Na2S
(2) 2NaCN + 2Na2S + 2H2O + O2 → 2NaSCN + 4NaOH
- Bước 2: Cho bột kẽm (Zn) vào dung dịch thu được xảy ra phản ứng
2Na[Ag(CN)2] + Zn → Na2[Zn(CN)4] + 2Ag
- Bước 3: Hòa tan hỗn hợp kim loại sau phản ứng trong H2SO4 loãng thu được kim loại Ag.
Biết các phản ứng xảy ra hoàn toàn, lượng Zn dùng dư 3% so với lượng cần thiết. Khi xử lí 1 tấn quặng argentite ở trên thì cần dùng bao nhiêu kg Zn? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
Quảng cáo
Trả lời:
Đáp án:
Đáp án: 234
⇒ mZn cần dùng = 3,5 · 103% · 65 ≈ 234 kg.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
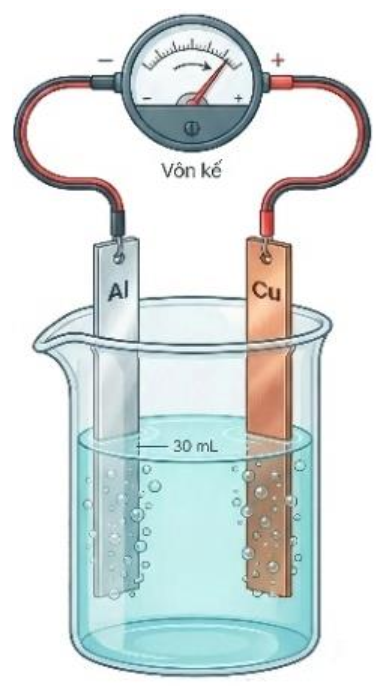
Ở bước 3, kim vôn kế chỉ 1,336 V.
Ở bước 3, khí chỉ thoát ra ở bề mặt lá đồng, còn lá nhôm không có khí thoát ra.
Ở bước 2, lá nhôm bị ăn mòn hóa học còn lá đồng không bị ăn mòn.
Ở bước 3, có sự tạo thành cặp pin điện hóa, trong đó lá nhôm là cathode và lá đồng là anode.
Lời giải
a. Sai. Ở bước 3, kim vôn kế chỉ 0,34 – (-1,676) = 2,016V.
b. Sai. Khí thoát ra ở cả hai điện cực.
c. Đúng
d. Sai. Lá nhôm là anode và lá đồng là cathode.
Lời giải
Đáp án: 135
\({n}_{{C}_{17}{H}_{35}COOH}=0,125;{n}_{{(C}_{17}{H}_{35}COO{)}_{3}{C}_{3}{H}_{5}}=\frac{\left. 1000-0,125.284 \right.}{890}=\frac{1929}{1780}mol\)
\({m}_{NaOH}=40.\left. 0,125+3.\frac{1929}{1780} \right.=135g\)
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Khi chuẩn độ, dung dịch KMnO4 có thể được cho vào bình tam giác, còn dung dịch H2O2 được cho vào burette.
Nồng độ mol của dung dịch H2O2 ban đầu xác định được là 0,0625 M.
Trong quá trình chuẩn độ, ion MnO4- bị oxi hoá thành Mn2+.
Nếu không thêm H2SO4, phản ứng sẽ tạo kết tủa nâu đen MnO2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.