Điện phân là một ứng dụng quan trọng của dòng điện trong việc biến đổi điện năng và hóa năng. Điện phân dung dịch NaCl có màng ngăn là phương pháp chủ đạo để sản xuất các hóa chất cơ bản như NaOH và chlorine (Cl2). Cho các phát biểu sau về quá trình điện phân dung dịch NaCl có màng ngăn, sử dụng các điện cực trơ:
(a) Tại cực dương (anode), xảy ra quá trình khử ion chloride thành khí chlorine.
(b) Tại cực âm (cathode), xảy ra quá trình oxi hóa nước tạo thành khí hydrogen và ion OH-.
(c) Dung dịch thu được trong quá trình điện phân có khả năng làm quỳ tím chuyển sang màu đỏ.
(d) Màng ngăn xốp có tác dụng ngăn không cho khí Cl2 tiếp xúc và phản ứng với dung dịch NaOH.
Số phát biểu đúng là:
1.
4.
3.
2.
Quảng cáo
Trả lời:
Đáp án đúng là A
(a) Sai, tại cực dương (anode) xảy ra quá trình oxi hóa Cl-: 2Cl- → Cl2 + 2e
(b) Sai, tại cực âm (cathode) xảy ra quá trình khử H2O: 2H2O + 2e → 2OH- + H2
(c) Sai, dung dịch thu được trong quá trình điện phân chứa OH- có khả năng làm quỳ tím chuyển sang màu xanh.
(d) Đúng
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Đinh sắt bị gỉ chủ yếu do sự ăn mòn hóa học.
Sau bước 1, trong dung dịch X chỉ chứa hai muối tan.
Phần trăm khối lượng sắt đã bị oxi hóa thành gỉ sắt là 10% (làm tròn đến hàng đơn vị).
Ở bước 1 và bước 3 đều xảy ra phản ứng oxi hóa - khử.
Lời giải
a) Sai, do đinh sắt là hợp kim Fe-C nên ăn mòn điện hóa học là chủ yếu.
b) Sai, X chứa 2 muối FeSO4, Fe2(SO4)3 tan và acid H2SO4 dư.
c) Đúng:
Trong 20 mL X chứa FeSO4 (a), Fe2(SO4)3 (b) và H2SO4 dư (a + 3b)
Với Ba(OH)2:
m↓ = 90a + 107.2b + 233(2a + 6b) = 14,4
Với KMnO4: nFe2+ = a = 0,046.0,1.5 = 0,023
→ b = 0,001
Trong 200 mL X chứa FeSO4 (0,23), Fe2(SO4)3 (0,01) và H2SO4 dư
nH2SO4 phản ứng = 0,23 + 0,01.3 = nH2 + nH2O
→ nO = nH2O = 0,0375 → nFe2O3 = 0,0125
→ %Fe bị oxi hóa = 0,0125.2/0,25 = 10%
d) Đúng, ở bước 1 có các phản ứng oxi hóa khử Fe + H+; Fe + Fe3+ và ở bước 3 là Fe2+ + H+ + MnO4-.
Lời giải
Đáp án:
Đáp án: 20
MY = 85/9
Tự chọn nY = 9 → mY = 85
nY = nX – 10%nX = 9 → nX = 10
Y chứa nNH3 = nX – nY = 1; nN2 = x; nH2 = y
nY = x + y + 1 = 9
mY = 28x + 2y + 17 = 85
→ x = 2; y = 6 (tỉ lệ 1 : 3 nên hiệu suất có thể tích theo N2 hoặc H2)
nN2 phản ứng = nNH3/2 = 0,5
nN2 ban đầu = x + 0,5 = 2,5
→ H = 0,5/2,5 = 20%
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
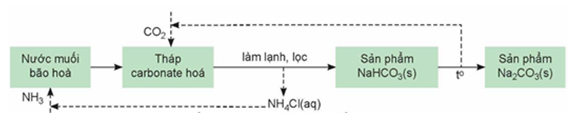
a. CaO thu được từ nhiệt phân đá vôi dùng để chuyển NH4Cl thành NH3.
b. Phản ứng xảy ra trong tháp carbonate hóa là: 2NaCl(aq) + 2NH3(aq) + H2O(l) + CO2(g) ⇌ Na2CO3(s) + 2NH4Cl(aq)
c. Nguyên liệu chính ban đầu của quá trình sản xuất soda bằng phương pháp Solvay là: NaCl, NH3, CaCO3 và H2O.
d. Để tiết kiệm chi phí, có thể thay thế dung dịch NaCl bão hòa bằng nước biển.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
carboxylic acid.
ester.
aldehyde.
ketone.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
a. Công thức phân tử của acetic acid là C2H6O2.
b. Giấm ăn có pH < 7.
c. Có thể dùng giấm ăn để làm mất mùi tanh của cá khi ta chế biến các món ăn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.