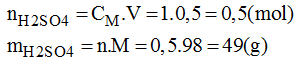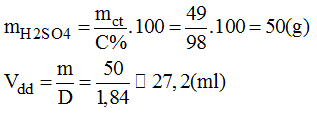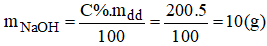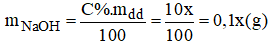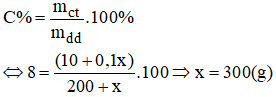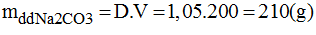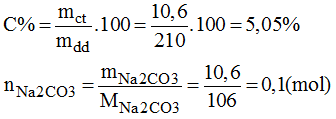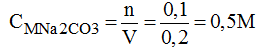Hãy tính toán và trình bày cách pha chế 0,5lit dung dịch có nồng độ 1mol/l từ có nồng độ 98%, khối lượng riêng là 1,84g/ml.
Câu hỏi trong đề: Giải Sách Bài Tập Hóa 8 !!
Quảng cáo
Trả lời:
* Số mol của cần để pha chế 500ml dung dịch 1M:
* Khối lượng 98% có chứa 49g :
* Cách pha chế: Đổ khoảng 400ml nước cất vào cốc có chia độ có dung tích khoảng 1lit. Rót từ từ 27,2ml 98% vào cốc khuấy đều. Sau đó thêm dần dần nước cất vào cốc cho đủ 500ml. ta pha chế được 500ml dung dịch 1M.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Khối lượng NaOH có trong dung dịch ban đầu:
Gọi x(g) là khối lượng dung dịch NaOH 10% cần dùng:
Đề thu được dung dịch 8% ta có:
Vậy phải trộn thêm 300g dung dịch NaOH 10% ta sẽ có 500(g) dung dịch NaOH nồng độ 8%.
Lời giải
Nồng độ phần trăm của dung dịch pha chế:
Nồng độ mol của dung dịch:
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.