Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe, Fe3O4, FeCO3 vào dung dịch hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2, NO, NO2, H2) có tỷ khối hơi so với H2 là 14,6 và dung dịch Z chỉ chứa các muối trung hòa với tổng khối lượng là m gam. Cho BaCl2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác, cho NaOH dư vào Z thì thấy có 1,085 mol NaOH phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Các phản ứng xảy ra hoàn toàn.
Cho các kết luận sau:
(a) Giá trị của m là 82,285 gam.
(b) Số mol của KNO3 trong dung dịch ban đầu là 0,225 mol.
(c) Phần trăm khối lượng của FeCO3 trong hỗn hợp X là 18,638 .
(d) Số mol của Fe3O4 trong X là 0,05 mol.
(e) Số mol của Mg trong X là 0,15 mol.
Số kết luận không đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Quảng cáo
Trả lời:
Chọn đáp án D
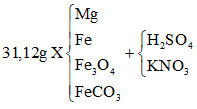
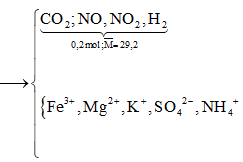
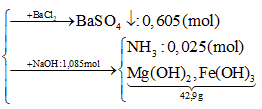
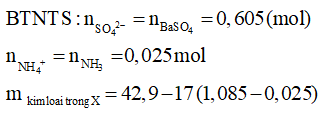 = 24,88 gam
= 24,88 gam
Quy đổi hỗn hợp X thành Fe, Mg, O và CO2
Đặt a, b là số mol của O và CO2 trong X. Đặt x là số mol H2
∑ m(O +CO2) = 31,12 – 24,88 = 6,24 (1)
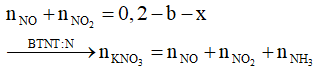
= 0,255 - b - x
Sau phản ứng với dung dịch NaOH thu được dd chứa K2SO4 và Na2SO4
Bảo toàn điện tích:
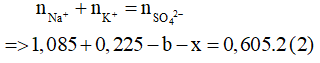
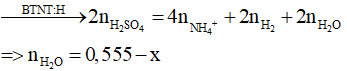
![]()
![]()
=> 31,12 + 0,605.98 + 101(0,255 - b - x) = 24,88 + 39(0,255 - b - x) + 0,025.18 + 0,605.96 + 0,2.29,2 + 18(0,55 - x)
=> 62 + 44x = 6,98 (3)
Từ (1), (2) và (3)
=> a = 0,28 (mol) ; b = 0,04 (mol) ; x = 0,06 (mol
=> m = 24,88 + 39 ( 0,255 –b –x) + 0,025.18 + 0,605.96 = 88, 285 => nhận định a) sai
nKNO3 = 0,225 – b – x = 0,125 => nhận định b) sai
%FeCO3 = ( 0,04.116/ 31,12).100% = 14,91% => nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => nhận định d) sai
=> có tất cả 4 nhận định sai.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
A. 1,6 gam
B. 3,2 gam
C. 6,4 gam
D. 12,8 gam
Lời giải
Chọn đáp án A
![]()
![]()
Do sau phản ứng thu được m gam chất rắn( chính là Cu) nên Fe chỉ tạo muối Fe2+
3Fe + 2NO3- + 8H+ → 3Fe2+ + 2NO↑+ 4H2O (1)
0,075 ← 0,2 (mol)
=> Sau phản ứng (1) số mol Fe dư là 0,1 – 0,075 = 0,025 (mol)
Fe + Cu2+ → Fe2+ + Cu↓
0,025 → 0,025 → 0,025 (mol)
m↓ = mCu = 0,025.64 = 1,6 (g) => chọn A
Ghi nhớ: NO3- trong môi trường H+ có tính oxi hóa như axit HNO3
Lời giải
Đáp án A
Chú ý: Al, Fe, Cr bị thụ động trong HNO3 đặc nguội.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. 2,39%.
B. 3,12%.
C. 4,20%.
D. 5,64%.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Thành phần chính của gỉ sắt là Fe3O4. xH2O.
B. Thành phần chính của gỉ đồng là Cu(OH)2. CuCO3.
C. Các đồ dùng bằng sắt thường bị ăn mòn do không được chế tạo từ Fe tinh khiết mà thường có lẫn các tạp chất khác.
D. Trong quá trình tạo thành gỉ Fe, ở catot xảy ra quá trình O2 + 2H2O + 4e → 4OH-
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. 100ml.
B. 200ml.
C. 300ml.
D. 400ml.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















