Cho hỗn hợp gồm 0,56 gam Fe và 0,96 gam Cu vào 200 ml dung dịch chứa hỗn hợp gồm H2SO40,5M và KNO30,2M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Giá trị tối thiểu của V là
A. 180.
B. 240.
C. 360.
D. 120.
Câu hỏi trong đề: Bộ 12 Đề thi Hóa học 11 Giữa kì 1 có đáp án !!
Quảng cáo
Trả lời:
Đáp án đúng là: A
Ta có: nFe= 0,01 mol; nCu= 0,015 mol; 
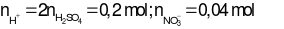
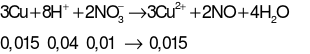 (1)
(1)
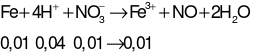 (2)
(2)
Tổng số mol H+tham gia phản ứng (1) và (2) là 0,08 mol
→ H+dư 0,2 – 0,08 = 0,12 mol
Dung dịch X có chứa Cu2+(0,015 mol), Fe3+(0,01 mol) và H+(0,12 mol)
H++ OH-→ H2O
Cu2++ 2OH-→ Cu(OH)2
Fe3++ 3OH-→ Fe(OH)3
\( \to {n_{O{H^ - }}} = {n_{{H^ + }}} + 2{n_{C{u^{2 + }}}} + 3{n_{F{e^{3 + }}}} = 0,12 + 2.0,015 + 3.0,01 = 0,18\,\,mol = {n_{NaOH}}\)
→ V = 0,18 lít = 180 ml
Hot: 1000+ Đề thi giữa kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
- Trọng tâm Hóa học 11 dùng cho cả 3 bộ sách Kết nối, Cánh diều, Chân trời sáng tạo VietJack - Sách 2025 ( 58.000₫ )
- Sách - Sổ tay kiến thức trọng tâm Vật lí 11 VietJack - Sách 2025 theo chương trình mới cho 2k8 ( 45.000₫ )
- Sách lớp 11 - Trọng tâm Toán, Lý, Hóa, Sử, Địa lớp 11 3 bộ sách KNTT, CTST, CD VietJack ( 52.000₫ )
- Sách lớp 10 - Combo Trọng tâm Toán, Văn, Anh và Lí, Hóa, Sinh cho cả 3 bộ KNTT, CD, CTST VietJack ( 75.000₫ )
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án đúng là: D
Khi cho P2O5vào nước có phản ứng:
P2O5+ 3H2O → 2H3PO4
Do đó để bài toán trở nên đơn giản, ta coi bài toán như phản ứng của H3PO4với dung dịch kiềm:
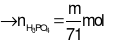
Các trường hợp có thể xảy ra:
+ TH1: NaOH và H3PO4phản ứng vừa đủ tạo muối
Khi đó 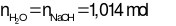
Áp dụng định luật bảo toàn khối lượng ta có: \({m_{{H_3}P{O_4}}} + {m_{NaOH}} = {m_{muoi}} + {m_{{H_2}O}}\)
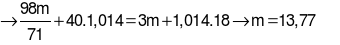
 NaOH dư
NaOH dư
Do đó trường hợp này không thỏa mãn
+ TH2: Chất rắn thu được gồm Na3PO4và NaOH dư
Có phản ứng xảy ra như sau:
H3PO4+ 3NaOH → Na3PO4+ 3H2O
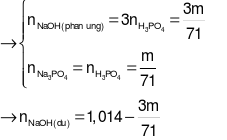
Do đó:
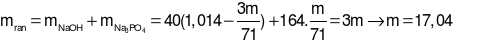
Câu 2
A. HCl.
B. NaOH.
C. NaCl.
D. NaNO3.
Lời giải
Đáp án đúng là: A
Dung dịch HCl là dung dịch axit, làm quỳ tím chuyển sang màu đỏ.
HCl → H++ Cl-
Câu 3
A.Tính oxi hóa rất mạnh của photpho đỏ.
B. Tính khử rất mạnh của photpho trắng.
C. Photpho trắng kém bền với nhiệt hơn photpho đỏ.
D. Khả năng phản ứng của photpho với kim loại sắt.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A.Cốc 1 chứa dung dịch NaOH.
B. Cốc 2 chứa nước cất.
C. Cốc 3 chứa dung dịch HCl.
D. Cốc 4 chứa axit axetic.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. 50.
B. 25.
C. 100.
D. 200.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A. 5.
B. 3.
C. 2.
D. 4.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
A. Na2CO3.
B. H2SO4.
C. AlCl3.
D. NaHCO3.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.