Đốt cháy hoàn toàn 0,1 mol chất hữu cơ A cần 12,8 gam O2. Sau phản ứng thu được 16,8 lít hỗn hợp hơi (136oC; 1atm) gồm CO2và hơi nước. Hỗn hợp này có tỷ khối so với CH4là 2,1.
Xác định công thức cấu tạo của A và gọi tên A biết rằng A tạo kết tủa vàng khi cho tác dụng với dung dịch AgNO3trong NH3. Tính lượng kết tủa khi cho 0,1 mol A phản ứng với hiệu suất 90%.
Câu hỏi trong đề: Bộ 12 Đề thi cuối kì 2 Hóa 11 có đáp án !!
Quảng cáo
Trả lời:
Hướng dẫn giải
Sơ đồ phản ứng: A + O2 CO2+ H2O.
CO2+ H2O.
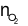 = 0,4 (mol).
= 0,4 (mol).
 =
= 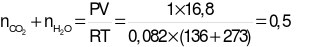 (mol).
(mol).
→  = 0,5(2,116) = 16,8 (gam).
= 0,5(2,116) = 16,8 (gam).
Gọi số mol CO2và số mol H2O lần lượt là x, y (mol).
Ta có hệ phương trình:
 .
.
Bảo toàn khối lượng:
mA+ 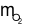 =
= 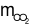 +
+ 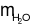 → mA+ 12,8 = 16,8 → mA= 4 (gam).
→ mA+ 12,8 = 16,8 → mA= 4 (gam).
mO(A)= mA– (mC+ mH) = 4 – (0,312 + 0,22) = 0 (gam).
→ Trong phân tử A chỉ gồm 2 nguyên tố C và H.
Số C = 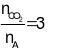 ; Số H =
; Số H =  .
.
→ Công thức phân tử của A là C3H4.
A tạo kết tủa vàng khi cho tác dụng với dung dịch AgNO3trong NH3
→ Công thức cấu tạo của A là: CH≡C-CH3.
Sơ đồ phản ứng: CH≡C-CH3 CAg≡C-CH3↓.
CAg≡C-CH3↓.
0,1 0,1 (mol)
→ m↓= 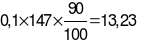 (gam).
(gam).
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
A.KOH, HF, Ca(NO3)2.
B.CH3COONa, HCl, NaOH.
C.NaCl, H2S, CH3COONa.
D.H2SO4, NaCl , H3PO4.
Lời giải
Đáp án đúng là: B
Chất điện li mạnh là những chất khi tan trong nước, các phân tử hòa tan đều phân li ra ion.
Những chất điện li mạnh là các axit mạnh như HCl, HNO3, HClO4, H2SO4…; các bazơ mạnh như NaOH, KOH, Ba(OH)2, Ca(OH)2, … và hầu hết các muối.
Dãy gồm những chất điện li mạnh là: CH3COONa, HCl, NaOH.
Loại A vì HF là chất điện li yếu.
Loại C vì H2S là chất điện li yếu.
Loại D vì H3PO4là chất điện li yếu.
Lời giải
Hướng dẫn giải
a) 2-metyl propen tác dụng với hiđro, đun nóng ( xúc tác Ni):
CH2=C(CH3)-CH3+ H2 CH3-CH(CH3)-CH3
CH3-CH(CH3)-CH3
b) axetilen tác dụng với nước:
CH≡CH + H2O 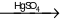 CH3CHO
CH3CHO
c) propin tác dụng với dung dịch AgNO3/NH3
CH≡C-CH3+ AgNO3+ NH3→ CAg≡ C-CH3↓ + NH4NO3
d) popen tác dụng với dung dịch KMnO4
3CH2=CH-CH3+ 2KMnO4+ 4H2O → 3CH2(OH)-CH(OH)-CH3+ 2KOH + 2MnO2
Câu 3
A.NaOH khan.
B.P2O5khan.
C.H2SO4đặc.
D.CuSO4khan.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
A.CH3COOH.
B.(NH4)2CO3.
C.CH3Cl.
D.C6H5NH2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















