Cho dãy các oxide sau Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
a) Độ phân cực của các liên kết trong dãy các oxide trên thay đổi thế nào?
b) Dựa vào giá trị độ âm điện của các nguyên tố trong Bảng 6.2, cho biết loại liên kết (ion, cộng hoá trị phân cực, cộng hóa trị không phân cực) trong từng phân tử oxide.
Cho dãy các oxide sau Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
a) Độ phân cực của các liên kết trong dãy các oxide trên thay đổi thế nào?
b) Dựa vào giá trị độ âm điện của các nguyên tố trong Bảng 6.2, cho biết loại liên kết (ion, cộng hoá trị phân cực, cộng hóa trị không phân cực) trong từng phân tử oxide.
Câu hỏi trong đề: Bài tập Ôn tập chương 3 có đáp án !!
Quảng cáo
Trả lời:
a) Độ phân cực trong dãy oxide giảm dần theo chiều từ trái sang phải:
Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Do hiệu độ âm điện giảm dần.
b) Hiệu độ âm điện của nguyên tố kim loại với oxi là:
Na2O: |∆χNa - O| = 2,51 ⇒ Liên kết giữa Na và O là liên kết ion.
MgO: |∆χMg - O| = 2,13 ⇒ Liên kết giữa Mg và O là liên kết ion.
Al2O3: |∆χAl - O| = 1,83 ⇒ Liên kết giữa Al và O là liên kết ion.
SiO2: |∆χSi - O| = 1,54 ⇒ Liên kết giữa Si và O là liên kết cộng hóa trị có cực
P2O5: |∆χP - O| = 1,25 ⇒ Liên kết giữa P và O là liên kết cộng hóa trị có cực
SO3: |∆χS - O| = 0,86 ⇒ Liên kết giữa S và O là liên kết cộng hóa trị có cực
Cl2O7: |∆χCl - O| = 0,28 ⇒ Liên kết giữa Cl và O là liên kết cộng hóa trị không cực
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
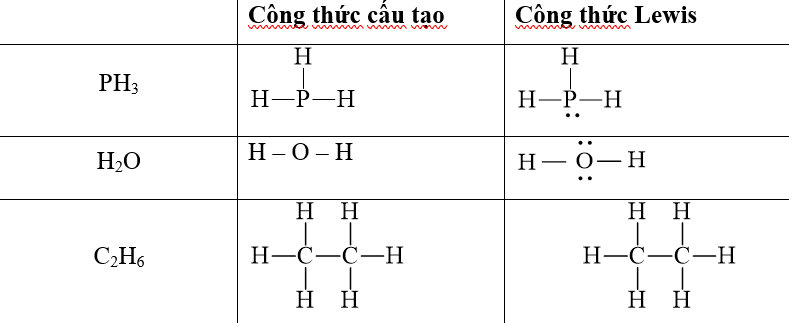
- Các nguyên tử O, P, N đều tạo liên kết phân cực với H, trong đó nguyên tử O có độ âm điện lớn hơn cả nên liên kết O – H sẽ phân cực nhất.
⇒ Phân tử H2O có liên kết phân cực mạnh nhất.
Lời giải
Trong phân tử CH4, hiệu độ âm điện của C và H: 2,55 – 2,2 = 0,35
⇒ Liên kết giữa C và H là liên kết cộng hóa trị không phân cực.
Trong phân tử CaCl2, hiệu độ âm điện của Ca và Cl: 3,16 – 1 = 2,16
⇒ Liên kết giữa Ca và Cl là liên kết ion.
Trong phân tử HBr, hiệu độ âm điện của H và Br: 2,96 – 2,2 = 0,76
⇒ Liên kết giữa H và Br là liên kết cộng hóa trị phân cực.
Trong phân tử NH3, hiệu độ âm điện của N và H: 3,04 – 2,2 = 0,84
⇒ Liên kết giữa N và H là liên kết cộng hóa trị phân cực.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















